Introduction
인삼은 오갈피나무과에 속하는 다년생 초본식물로서 작물의 특성상 동일 장소에서 3-5년 동안 장기간 재배하므로 작물의 생육기간 중 기상, 재배환경 및 병충해 등에 의한 피해를 받기 쉽다. 특히, 장기간의 재배기간 중 점무늬병, 탄저병, 잿빛곰팡이병, 뿌리썩음병 등의 각종 병해에 의해 매년 30-60%의 수량 감소피해를 입는 것으로 알려져 있어, 이러한 병해 피해를 효과적으로 예방할 수 있는 친환경 농자재 개발이 필요한 실정이다 (Kim et al., 2012).
인삼 점무늬병은 Alternaria panax, Alternaria sp. 균에 의해 유발되어 인삼의 줄기, 잎 또는 열매 등에 흑갈색의 부정형 병반이 형성되는 병으로, 인삼 지상부에서 발생하는 병 중 가장 발생빈도가 높으며 발병 시 가장 많은 수량 감소피해를 초래한다 (Bae et al., 2005). 인삼 점무늬병은 주로 4월부터 8월까지 발생하며, 발생 정도는 강우시기, 기간 및 강우량 등과 밀접한 관련이 있는 것으로 알려져 있다 (Oh et al., 1987; Kang et al., 2007). 인삼 점무늬병 중 줄기점무늬병은 4월 하순부터 발생하기 시작하여 5월 중순 이후부터는 감소하며, 잎점무늬병은 5월 중순부터 발생이 증가하여 저년생에서는 6월 중순에 가장 많이 발생한다. 또한, 저년생보다는 고년생에서 심하게 발생하며 수분에 잘 노출되는 전주에서 더 많이 발생한다 (Cho et al., 1998).
점무늬병, 잿빛곰팡이병 등 인삼에서 발생되는 병해 방제를 위해서 물리적 방제, 경종적 방제 및 화학적 방제 등 여러 방제방법을 이용하고 있으나, 대부분 사용이 편하고 효과가 빠른 화학적 방제방법을 주로 사용하고 있다 (Lee et al., 2008). 최근 화학농약의 오남용으로 인한 토양, 수질 등 환경오염 부작용 및 농산물의 안전성에 대한 우려로 잔류농약에 대한 규제가 점차 엄격해지고 있는 추세이다. 이에 따라, 인삼재배농가에서 농약 잔류에 대한 우려 없이 사용할 수 있도록 화학농약을 대체할 수 있는 친환경 농자재 개발에 대한 요구가 점점 커지고 있다 (Lee, 2012).
이와 같이, 친환경 농자재에 대한 관심과 수요가 증가함에 따라 인삼 뿌리썩음병, 모잘록병 등 뿌리부위에서 발생되는 지하부병과 점무늬병, 탄저병 등 잎, 줄기부위에서 발생되는 지상부병의 친환경 방제를 위해 Cylindrocarpon destructans, Fusarium solani, Rhizoctonia solani, Pythium spp, Alternaria panax 등 발병 원인균에 대해 길항활성이 있는 미생물을 활용하기 위한 연구가 활발히 진행되고 있다 (Lee et al., 2008; Kim et al., 2012; Lee et al., 2012; Kim and Park, 2013; Lim et al., 2014; Lee et al., 2017).
본 연구는 인삼 재배 시 인삼 지상부병 중 발생빈도가 높으며 가장 큰 생산량 감소를 일으키는 점무늬병 방제를 위해 인삼 재배지 토양으로부터 선발한 길항미생물의 화학농약 대체 가능성을 분석하고 친환경 농자재로의 개발 가능성을 확인하고자 수행하였다.
Materials and Methods
균주 분리
인삼 점무늬병 원인균 (Alternaria panax)에 길항활성을 가진 미생물 분리를 위해, 강원도 철원군 근남면 인삼 재배지 표토층 아래 10 cm 깊이의 토양을 채취하였다. 채취한 토양 1 g을 9 mL의 멸균수에 넣고 25°C, 100 rpm 조건으로 30분 동안 진탕 후 십진희석한 다음 미리 준비해 놓은 TSA (Tryptic soy agar, Difco, USA) 배지에 200 µl씩 도말하여 30°C에서 24-48시간 동안 배양하였다. TSA배지에서 자라난 단일 콜로니를 분리하여 사면배지에서 보존하면서 인삼 병원균에 대한 길항활성을 검정하였다.
항균활성 검정
토양에서 분리한 KL87 균주의 인삼 점무늬병 병원균에 대한 길항활성을 확인하기 위하여, PDA (Potato dextrose agar, Difco, USA)배지에서 25°C, 10일간 배양한 A. panax 균의 균총 가장자리를 cork borer로 떼어낸 후 PDA 배지가 들어있는 페트리디쉬에 접종하였다. A. panax 균을 접종한 지점에서 2.5 cm 떨어진 PDA 배지 위에 LB broth (tryptone 10 g, yeast extract 5 g, sodium chloride 10 g L-1)에서 2일 동안 배양한 분리균주 콜로니를 멸균수에 희석하여 105 CFU/ml 농도로 조절한 다음, 희석한 현탁액 10 µl를 paper disk에 접종하였다. 항균활성 검정을 위한 A. panax 균주는 농업유전자원센터에서 분양받아 보존하면서 사용하였으며, 토양에서 분리한 균주의 길항력은 25°C에서 10일간 배양한 후 나타난 저지원 (Inhibition zone)의 크기로 확인하였다.
균주 동정
인삼 점무늬병원균에 대한 길항활성을 나타내는 KL87 균주의 동정을 위해 유전적 특성과 생화학적 특성을 분석하였다. 유전적 특성은 16S rRNA 유전자 분석을 수행하였으며, 균주를 LB 배지에서 배양 후 8,000 rpm으로 10분간 원심 분리하여 균체를 수확한 다음, 균체 50 mg을 Genomic DNA Prep Kit (Solgent, Daejeon, Korea)를 이용하여 genomic DNA를 추출하였다. 16S rRNA 유전자 증폭은 universal primer인 27F (5'-AGAGTTTGATCATGGCTCAG-3')와 1492R (5'-GGATACCTTGTTA-CGACTT-3')을 이용하였다. PCR 반응은 정방향 프라이머 (27F) 1 µl, 역방향 프라이머 (1492R) 1 µl, DNA 20 ng/µl, 4dNTP (10 mM) 2µl, 10× Taq 버퍼 2.5 µl, solgent EF Tag 0.3 µl, 멸균수 17.2 µl가 혼합된 총 25 µl의 PCR 혼합 반응액을 94°C, 20초 동안 가열하여 DNA의 변성을 유도하였다. 변성 유도 후에는 반응온도를 50°C로 낮추어 프라이머가 일치하는 sequence에 결합할 수 있도록 40초 동안 반응시켰으며, 이후 72°C에서 온도를 높여 DNA 복제를 1분 30초 동안 유도하는 주기 (cycle)를 1cycle로 하여 30 cycle을 실시하였다. 염기서열 분석은 Solgent Co. (Daejeon, Korea)에 의뢰하여 분석하였으며, 바실러스속 표준균주의 염기서열은 미국 국립생물정보센터 (National Center for Biotechnology Information)에서 받아 MEGA 4.0 program으로 계통도를 작성하였다 (Tamura et al., 2011). 계통도는 neighbor joining 알고리즘을 이용하여 작성하였고 Bootstrapping을 1,000회 반복하여 견고성을 확인하였다. 길항균주의 생화학적 특성은 Vitek2 compact system (bioMérieux, France)을 이용하여 46가지의 특성을 분석하였다. 순수 배양된 균주를 0.45% NaCl이 함유되어 있는 생리식염수에 혼합하여 Vitek densichek (bioMérieux, France)로 탁도 2 McFarland로 현탁한 후, BCL card (bioMérieux, France)에 분주하여 Vitek2 system에서 생화학 특성을 분석하였으며, 생화학 특성 분석 후 Vitek2 Advanced Expert System (AES) software로 판독하여 균주를 동정하였다 (Lim et al., 2015).
인삼 점무늬병 방제효과 검정
선발한 KL87 균주의 인삼 재배지에서의 점무늬병 발생 억제효과 검정을 위해 시험시료를 다음과 같이 제조하였다. 시험균주를 LB broth (Difco, USA)에 접종한 다음 진탕배양기 (SK-760M, Jeiotech, Korea)에서 25°C, 120 rpm 조건으로 3일 동안 배양하여 얻은 배양액에 skim milk (Difco, USA) 10%를 넣고 5일 동안 동결건조하였다 (FD8508, Ilshin, Korea). 동결건조한 KL87균주의 생균수는 동결건조한 시료 1 g을 단계별로 희석한 후 배양한 다음 균수를 조사하여 측정하였으며, 점무늬병 발생 억제효과는 동결건조한 시험균주를 1.0×105 CFU/mL농도로 희석하여 사용하였다. KL87 균주의 인삼 점무늬병 방제효과 검정시험은 4년근 인삼 재배지에서 수행하였으며 5월 하순에서 7월 상순 사이 재배면적 1.62 m2당 균주 희석액 1 L씩을 10-15일 간격으로 4회 엽면살포하였다. 방제효과 비교를 위한 대조구는 Polyoxin B 1,000배 희석액, Mancozeb 600배 희석액 및 Polyoxin D 1,000배 희석액을 5월 하순에서 7월 상순 사이 재배면적 1.62 m2당 1 L씩 4회 교호살포하였으며, 방제효과는 점무늬병 이병엽을 조사하여 방제가 (%)를 아래의 공식에 따라 계산하여 최종 분석하였다.
방제가 (%) = {(무처리군 발병도 - 방제처리군 발병도) ÷ 무처리군 발병도} × 100
Results and Discussion
균주 분리 및 항균활성 검정
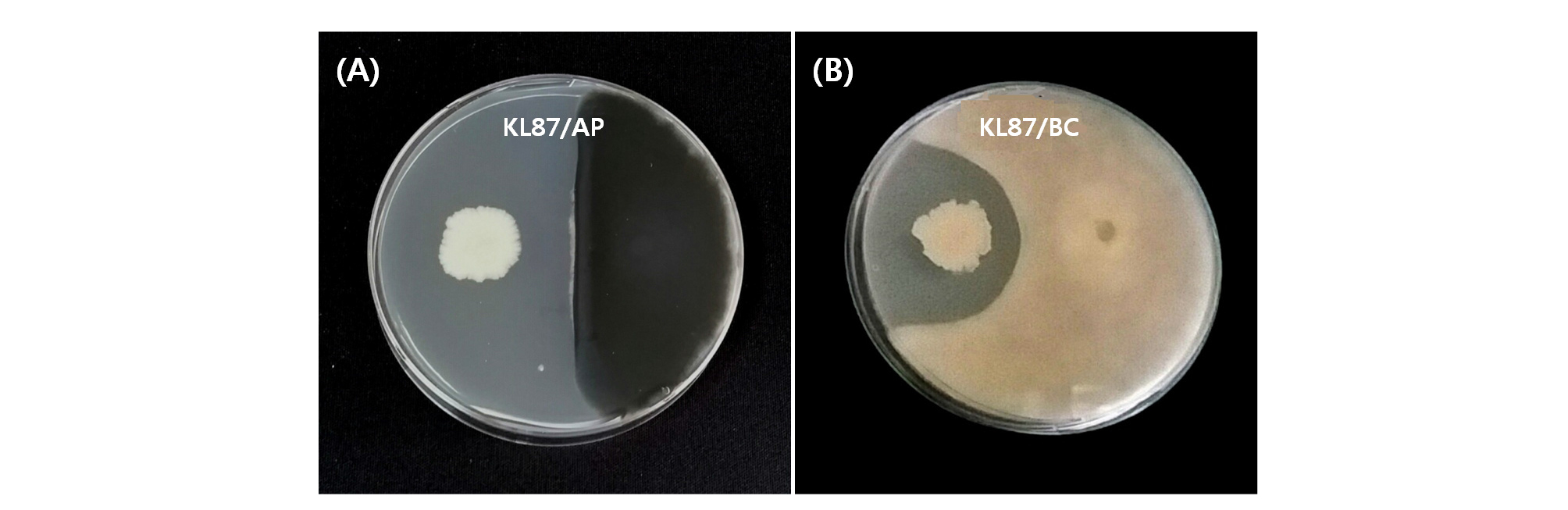
인삼 점무늬병 방제를 위한 길항균 선발을 위해 인삼재배지 토양시료에서 260여 균주를 분리하여 인삼 점무늬병 원인균 (A. panax)에 대한 각 균주의 항균활성을 조사하였다. 분리한 균주 중 34개의 균주가 점무늬병원균의 생장을 억제하는 효과를 가지고 있었으며 (data not shown), 이 중 항균활성이 우수한 KL87균주를 최종 선발하여 유전적 특성 및 생화학적 특성을 분석하였다. KL87균주는 인삼 점무늬병원균인 A. panax균의 생장을 강하게 억제할 뿐만 아니라 인삼 잿빛곰팡이병원균 Botrytis cinerea의 생장도 억제하는 활성을 가지고 있었다 (Fig. 1). 잿빛곰팡이병은 인삼 재배 시 잎과 지제부 줄기 등에 발생하여 큰 피해를 입히는 병으로, 7월 중순부터 발병하여 8월 중순 이후에는 발병율이 높아지는 주요 병해로서 (RDA, 2009), KL87 균주는 인삼 재배 시 발생하는 점무늬병 및 잿빛곰팡이병 등 주요 지상부병을 동시에 효과적으로 방제할 수 있을 것으로 판단되며, KL87 균주를 이용한 친환경 방제제 개발 가능성을 확인할 수 있었다.
분리 균주 동정
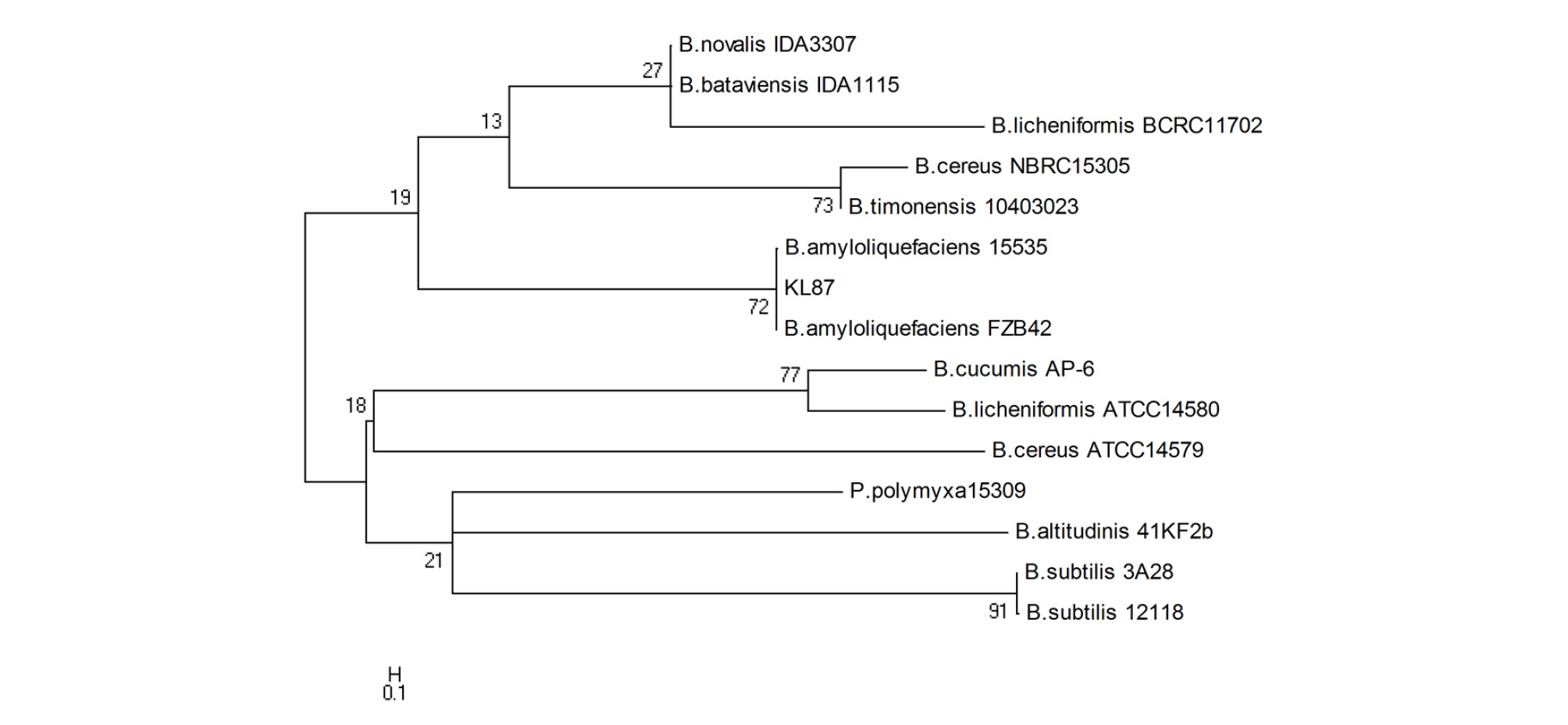
인삼 점무늬병원균에 길항활성이 있는 KL87 균주의 정확한 동정을 위해 16S ribosomal RNA 유전자 염기서열을 분석한 후 분자계통도를 작성하였다. KL87 균주는 Bacillus amyloliquefaciens subsp. plantarum strain FZB42 및 Bacillus amyloliquefaciens strain NBRC15535와 99%의 높은 상동성을 보였으며, 염기서열을 바탕으로 한 계통수 분석 결과, Bootstrap 값이 72%로 비교적 높은 것으로 확인되었다 (Fig. 2). 독성을 가진 항균성 물질을 분비하여 길항활성을 나타내는 것으로 알려져 있는 바실러스 (Bacillus)속 미생물을 이용하여 인삼 재배 시 수량 감소 피해를 야기하는 지상부병을 방제하기 위한 연구가 활발히 진행되고 있으며, Bacillus subtilis를 이용한 인삼 점무늬병 방제 (Lee et al., 2008), 인삼 점무늬병원균 (Alternaria panax)과 탄저병원균 (Colletotrichum gloeosporioides)에 대한 길항활성을 가진 Bacillus균 (Lee et al., 2012) 등이 보고된 바 있다. KL87 균주의 16S ribosomal RNA 염기서열을 분석한 결과, B. amyloliquefaciens와 높은 상동성을 보여 B. amyloliquefaciens속하는 균주인 것으로 추정되었으나, 정확한 균주 확인을 위하여 생화학적 특성을 분석하였다. Vitek 2 system을 이용한 생화학적 특성 검정 결과 (Table 1), KL87 균주는 β-xylosidase, Phenylalanine arylamidase 및 L-Pyrrolydonyl-arylamidase 등 18종류의 생화학 반응에서 양성을 나타냈으나 L-Lysine-arylamidase, L-Aspartate armylamidas 및 Leucine arylamidase 등 28 종류의 생화학 반응은 음성을 나타내어 Bacillus amyloliquefaciens와 99% 유사한 생화학적 특성을 가진 것으로 확인되었다 (Table 2). Bacillus amyloliquefaciens 균은 식물체의 뿌리 주위나 식물 내에서 흔하게 발견되는 미생물로서 고추역병균인 Phytophthora capsici의 생육을 억제하며 (Korea patent, 10-2002-0028954), 인삼 모잘록병원균인 Phytium ultimum과 Rhizoctonia solani의 생장 억제 활성을 가지고 있는 것으로 보고된 바 있고 (Park et al., 2016), 인삼 뿌리썩음병원균 (Cylindroncarpon destructans) 및 모잘록병원균 (Rhizoctonia solani) 등에도 항균활성이 있는 것으로 알려져 있다 (Kim et al., 2012; Jamal et al., 2015). 이와 같이, A. panax와 B. cinerea 생장 억제 활성을 가지고 있는 KL87균주는 유전적, 생화학적 특성 분석을 통해 Bacillus amyloliquefaciens 균으로 확인되었으며, Bacillus amyloliquefaciens 균은 여러 연구자들에 의해 식물 병원균에 대한 항균 효과가 우수한 것으로 보고되고 있어 친환경 농자재로 개발 시 인삼에서 발생하는 점무늬병 등의 지상부병을 효과적으로 방제할 수 있을 것으로 판단된다.
Table 1. Biochemical characteristics of KL87 strain.
Table 2. Identification of the isolated KL87 strain by Vitek2 system.
| Strain | Identification Result | Note | |
| Species | Probability | ||
| KL87 | Bacillus amyloliquefaciens | 99% | Identified |
인삼 점무늬병 방제효과 검정
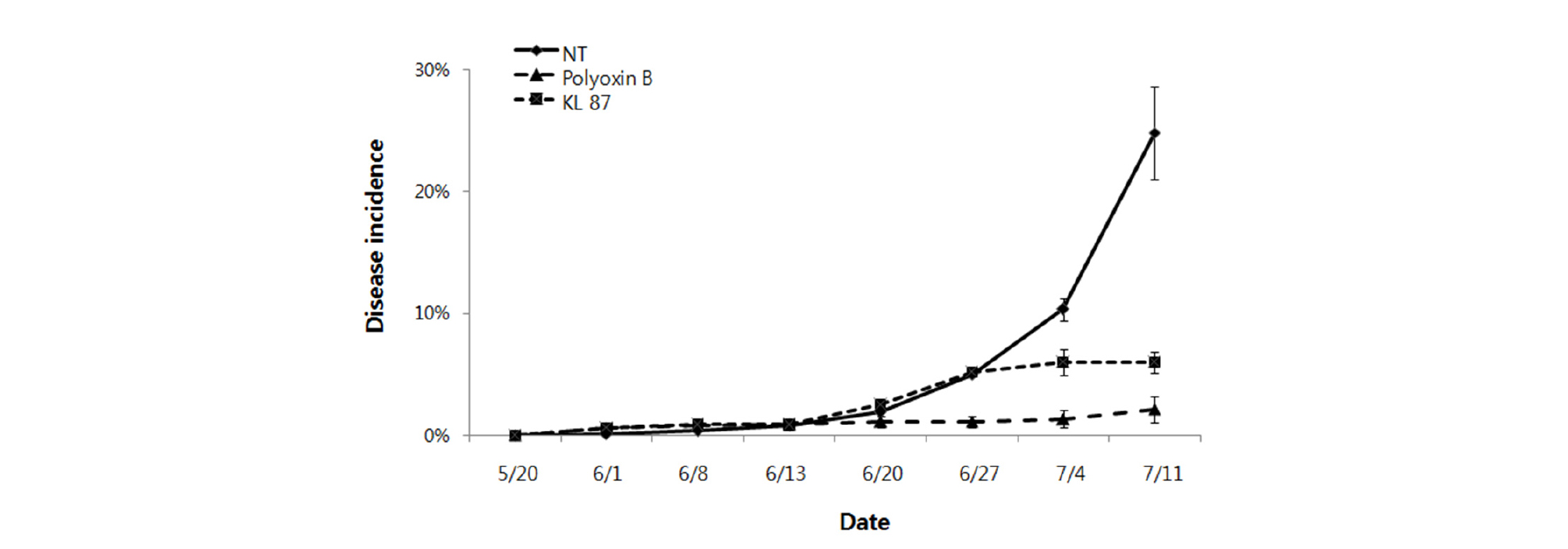
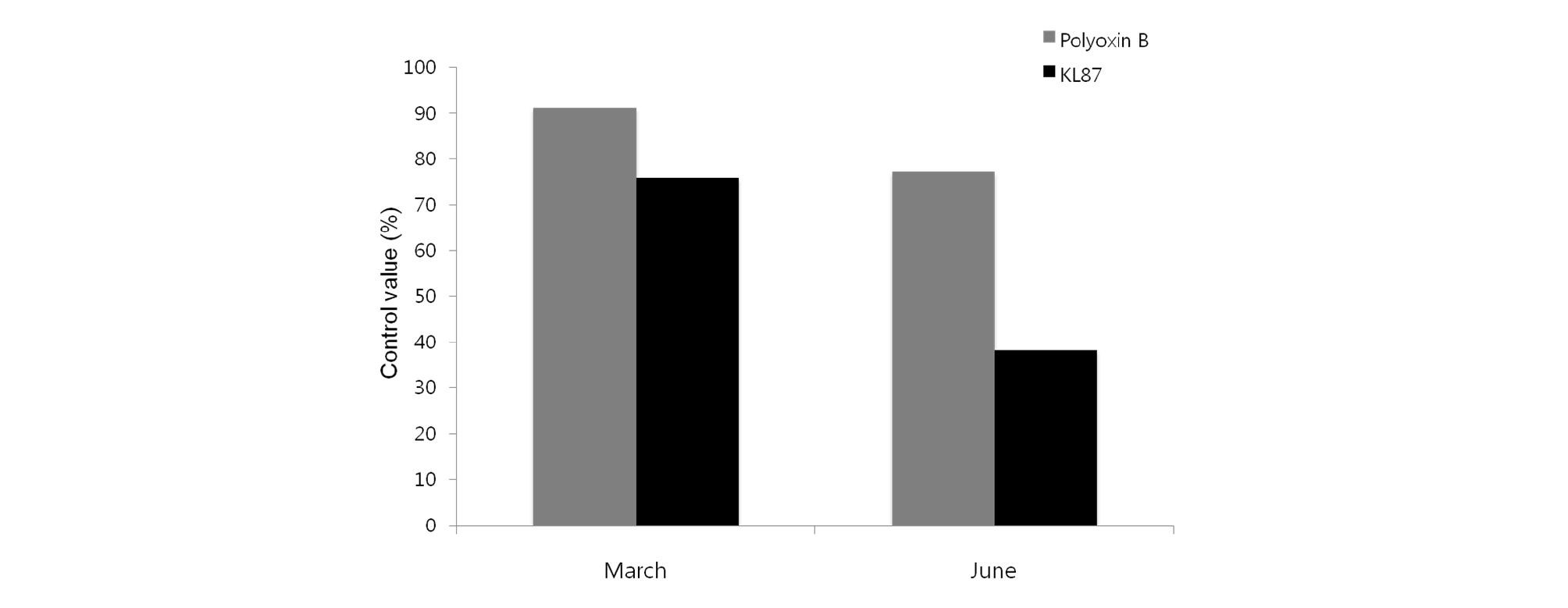
동결건조한 KL87 균주를 1.0×105 CFU/mL농도로 희석한 후 4년근 인삼 재배지에 5월부터 7월까지 10-15일 간격으로 총 4회 엽면살포한 후 점무늬병 발생 억제효과를 분석하였다. 점무늬병 방제효과 시험결과, 무처리구의 점무늬병 발병률은 24.8±3.8%였으나, Polyoxin B 1,000배액 등 화학농약을 교호살포한 시험구는 발병률이 2.2±1.1%로 91.3%의 방제효과를 나타냈으며, KL87 균주를 엽면살포한 시험구의 점무늬병 발병률은 6.0±0.9%로 무처리구 대비 75.9%의 방제효과를 나타냈다 (Fig. 3). KL87 균주의 인삼 점무늬병 방제효과는 화학농약 대비 83% 수준으로 효과가 매우 우수하여 친환경 농자재로의 개발 및 산업화 가능성을 확인할 수 있었다. KL87 균주의 처리 적기 확인을 위해 5월과 6월로 미생물제 처리시기에 차이를 두어 점무늬병 방제효과를 시험하였다. 시험결과, 5월부터 화학농약 처리 시 점무늬병 발병률은 2.2%로 무처리구의 24.8% 대비 91.3%의 방제효과를 나타냈으나, 6월 처리 시 77.2%의 방제효과를 나타내어 5월 처리구에 비해 방제효과가 14.1% 감소하였다. KL87 균주는 6월부터 처리 시 점무늬병 방제율이 38.2%로 5월 처리구 방제율 75.9%에 비해 큰 폭으로 감소하였으며, 이와 같은 결과로 보아 KL87 균주를 이용한 인삼 점무늬병의 효과적인 방제를 위해서는 발생초기인 5월부터 미생물제를 처리하는 것이 적절한 것으로 판단된다 (Fig. 4).
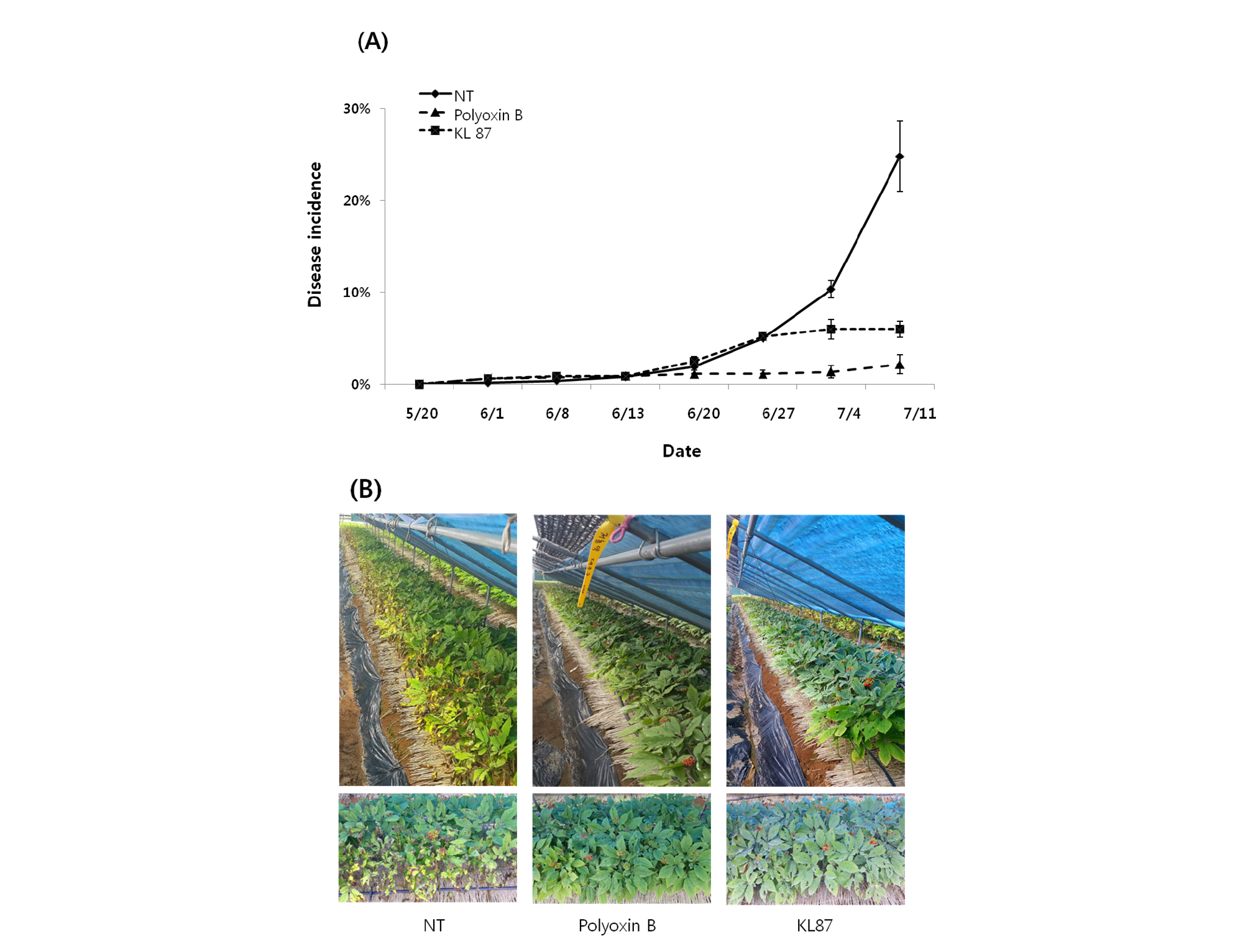
Fig. 3.
Suppressive effect of Bacillus amyloliquefaciens KL87 on Alternaria blight occurrence in the field of ginseng cultivation. NT: no treatment, Polyoxin B: alternate application (Polyoxin B, Mancozeb and Polyoxin D), KL87: treated with Bacillus amyloliquefaciens KL87 at a concentration of 1.0×105 CFU/mL.
최근, 안전 농산물 선호 및 잔류농약 규제 강화 추세에 따라 농약 잔류에 대한 우려 없이 사용할 수 있는 친환경 농자재 개발에 대한 연구가 활발히 진행되고 있다. 인삼 점무늬병 방제효과가 우수한 KL87 균주는 향후 균주 최적 배양을 위한 생리특성 및 방제효과를 최대화 할 수 있는 제형화 기술 등에 대한 추가적인 연구를 통해 농업현장에서 화학농약을 대체할 수 있는 친환경 농자재로 활용 가능할 것으로 사료된다.