Regression Model to Predict Nitrogen Mineralization Using Soil Parameters for Pepper Upland
ABSTRACT
Introduction
농업에서 질소는 작물 생산성을 위해 반드시 필요한 원소이나, 질소의 과다한 공급은 수계오염 등 환경부하의 원인이 된다. 그러나 농가에서는 대체로 적정량보다 많은 양의 비료, 부숙유기질비료 등을 사용하는 경향이 있으므로 토양의 이화학적 특성을 고려하여 적정량의 질소를 공급하도록 관리가 필요하다 (Kim et al., 2020).
토양 질소공급량은 투입하는 양분의 종류와 양에 주로 영향을 받는다. 작부체계에 따른 질소 비료와 유기물 공급량 차이는 토양 질소공급량에 영향을 미치며 (Carpenter-Boggs et al., 2000), 토양 질소 무기화량은 질소 비료공급량과 비례하여 증가한다 (Rasmussen et al., 1998). 또한 토양 유기태 질소의 무기화-부동화 과정은 유기물의 탄질률에 따라 달라진다 (Reddy et al., 1979). 따라서 작물 재배를 위한 적정 질소 공급량을 결정하기 위해서는 해당 농경지의 양분관리 이력을 고려해야 하며, 전작물 수확 후 또는 정식 전 토양 중 질소함량을 분석하는 것이 중요하다.
질소 공급량은 토양에서 용탈되는 무기태 질소량을 구하며, 시간에 따라 무기화되는 질소를 누적하여 kinetic model (Eq. 1)에 적용하면 토양의 잠재적 질소 무기화 예측식을 도출할 수 있다 (Stanford and Smith, 1972). N min은 시간에 따른 누적 질소 무기화량이고, N0는 잠재적으로 무기화될 수 있는 질소, k는 무기화 속도상수, t는 시간이다 (Campbell et al., 1993).
외국에서는 질소 비료 공급량 추천을 위해 토양 질소 무기화 계수와 작물 수량과의 관계를 분석한 사례들이 있으며 (Sharifi et al., 2007; Dessureault-Rompré et al., 2011), 토양 특성에 따른 질소무기화 계수를 예측하는 모델을 구하는 등 토양 질소 무기화량을 예측하는 다양한 연구들이 수행되었다 (Heumann et al., 2002; Bechtold and Naiman, 2006; Dessureault-Rompré et al., 2015).
국내에서는 Kim et al. (2005)이 논과 밭토양에 대하여 온도 수준별 질소 무기화 계수를 구한 바 있으나 토양 자체에 대한 질소 무기화를 연구한 사례는 많지 않다. 주로 단일 토양에서 유기자재 투입에 따른 질소 무기화 계수를 구하는 연구가 주로 수행되었기 때문에 (Yun et al., 2010; Shin et al., 2015), 우리나라 밭토양의 질소 무기화 예측 모델을 설정하기 위해서는 토양 질소 공급력에 대한 자료 구축이 필요한 실정이다.
본 연구는 우리나라 밭토양의 토양 특성별 질소 공급량을 예측하기 위하여 재배면적이 크고 재배기간이 약 4 - 5개월 이상으로 길어 상대적으로 양분 투입량이 많은 고추 재배 밭토양을 대상으로 질소 무기화 계수를 구하고, 토양 특성에 따라 질소 무기화 계수를 추정하는 다중선형회귀 식을 산정하였다.
Materials and Methods
토양시료 채취 및 질소 무기화 분석
질소 무기화 분석을 위해 충남 태안, 충남 청양 (2017년) 경북 영양, 전북 임실, 충북 괴산 (2018년)의 노지 고추 재배지 40 지점을 무작위로 선정하여 토양을 채취하였다. 비료와 퇴비를 시용하기 전인 3월 초에 표토에서 토심 10 cm 깊이까지 채취하고, 채취한 토양은 골고루 혼합하였다.
질소 무기화 실험은 Stanford and Smith (1972)의 방법을 적용하였으며, 실험방법은 Lee et al. (2019)와 동일하다. 토양 시료는 풍건하여 2 mm 체로 거른 후 질소 무기화량 분석을 위한 항온시험을 수행하였으며, 0.45μm filter가 장착된 150 mL 용량의 항온용기 (Corning, USA)에 토양 65 g을 넣고, 용적밀도는 1.2 g cm-3을 맞추었다. 토양수분은 포장용수량의 60%으로 맞추고 3일 간격으로 보정하였다. 온도는 유기물 분해가 가장 활발한 27°C를 기준으로 하였으며 (Gilmour et al., 1977), 항온 처리 후 1, 2, 4, 8, 10, 12, 16주에 질소 무기화량을 분석하였다. 질소 무기화량 측정을 위해 토양에 0.01 M CaCl2 용액을 100 mL를 주입하여 진공펌프로 토양용액을 침출하고, 용탈 후 N-free nutrient solution (0.002 M CaSO4, 0.002 M MgSO4, 0.005 M Ca(H2PO4)2, 0.0025 M K2SO4) 를 25 mL 넣어 완전히 용출시킨 후 다시 항온하였다.
시간에 따라 누적된 질소 무기화량으로 질소 무기화 계수를 구하였으며, 이 때 1주차의 질소 무기화량은 무기화 된 질소 (Mineralized N)로서 별도로 분리하였다 (Eq. 2). 질소 무기화 시험을 위해 건토에 수분을 처리할 때 무기태 질소 함량이 급격히 증가하여 질소 무기화 계수에 영향을 미칠 수 있기 때문이다 (Sharifi et al., 2007; Dessureault-Rompré et al., 2015).
토양 이화학성 분석
토성은 비중계법 (Gee and Bauder, 1986), CEC는 mechanical vacuum extractor를 이용하여 NH4OAC (pH 7.0) 침출법으로 분석하였다. 토양 pH와 EC는 토양과 증류수 비율을 1:5로 하여 pH, EC meter (Orion, Thermo scientific, USA) 로 측정하였고, 유기물은 Tyurin법, 총질소와 탄질률은 C/N analyzer (Vario MAX CNS, elementar, Germany) 로 분석하였다.
통계분석 및 질소 무기화 계수 예측 모델식에 토양검정 자료 적용
Kinetic model을 적용한 질소 무기화 계수 예측, 토양 이화학적 특성과 질소 무기화 계수의 상관관계, 질소 무기화 계수 예측을 위한 다중선형회귀 분석은 SAS 통계프로그램 (Ver.9.4, SAS Institute Inc., USA) 이용하였다.
질소 무기화 계수 예측 모델식을 적용했을 때 토양특성에 따른 질소 무기화량을 비교하기 위하여 전북 고추재배지의 2020년도 토양검정 자료를 이용하여 질소 무기화량을 예측하였다. 표토 토성이 사양토인 월곡통 (모래 55.1%, 점토 28.1%) 의 토양검정 자료 52점과 식양토인 전남통 (모래 28.8%, 점토 31.5%) 의 토양검정 자료 68점에 대하여 토양 유기물 함량과 EC에 따른 150일간 총 질소 무기화량을 비교하였다.
Results and Discussion
밭토양의 질소 무기화 계수
시험토양의 토성은 사양토, 양토, 미사질식양토에 해당되었으며, 토양 유기물 함량은 평균 27 g kg-1으로 국내 밭토양의 평균 유기물 함량과 일치하였다 (RDA, 2017). 또한 유기자재 및 비료 시용과 관련되는 총질소, 탄질률 등 토양 이화학성은 채취한 토양시료에 따라 다양하게 분포하였다 (Table 1).
Table 1.
Ranges of soil properties used for fitting the kinetic models (n=40).
|
Sand
|
Silt
|
Clay
|
CEC
|
pH
|
EC
|
SOM
|
T-N
|
C/N
|
|
(%)
|
(%)
|
(%)
|
(cmolc kg-1)
|
(1:5)
|
(dS m-1)
|
(g kg-1)
|
(g kg-1)
|
ratio
|
|
Average
|
48
|
40
|
13
|
20
|
6.0
|
1.8
|
27
|
1.8
|
10
|
|
Max
|
74
|
64
|
32
|
32
|
7.5
|
6.6
|
58
|
5.1
|
15
|
|
Min
|
8
|
20
|
3
|
3
|
4.4
|
0.4
|
6
|
0.4
|
9
|
|
CV*(%)
|
30
|
27
|
55
|
29
|
13
|
93
|
48
|
64
|
11
|
토양 질소 무기화량을 1차 kinetic model에 적용했을 때 결정계수 (R2)는 평균 0.966으로 질소 무기화 예측에 활용할 수 있을 정도로 상당히 높게 나타났다 (Table 2). 질소 무기화 항온실험 1주차에 분석된 무기태 질소 (Mineralized N) 는 평균 206 mg kg-1 이었으며, 용적밀도 1.2 g cm-3, 토심 10 cm 적용 시 약 24.7 kg 10a-1에 해당되는 양이었다 (Table 2). 노지 고추의 질소 표준사용량 (19 kg 10a-1) 과 비교할 때 비료와 퇴비 시용으로 인해 상당히 많은 양의 질소가 토양에 남아있다는 것이 실험적으로 확인되었다.
Table 2.
Average and range of soil nitrogen mineralization factors (Mineralized N, N0 and k) from fitting the first-order kinetic models at 27°C according to level of soil organic matter (n=40).
Soil organic matter
(g kg-1)
|
Mineralized N*
(mg kg-1)
|
N0
(mg kg-1)
|
k
(day-1)
|
R2 |
<20
(n=13)
|
65
(2 - 338)
|
35
(5 - 94)
|
0.039
(0.005 - 0.098)
|
0.967
(0.908 - 0.999)
|
20 - 30
(n=12)
|
188
(6 - 885)
|
81
(37 - 128)
|
0.036
(0.002 - 0.130)
|
0.969
(0.910 - 0.996)
|
30<
(n=15)
|
343
(17 - 937)
|
125
(2 - 335)
|
0.052
(0.001 - 0.160)
|
0.963
(0.795 - 0.998)
|
질소 무기화 계수인 Mineralized N, N0, k를 우리나라 밭토양의 질소 추천기준인 토양 유기물 함량을 기준으로 20 g kg-1 미만, 적정범위인 20 - 30 g kg-1, 30 g kg-1 초과로 구분하여 제시하였다. 토양 유기물이 낮은 토양에서 높은 토양 순서로 질소 무기화 계수를 비교하면, Mineralized N의 평균값은 각각 65, 188, 343 mg kg-1 이었고, N0 평균값은 각각 35, 81, 125 mg kg-1으로 토양 유기물 함량이 많을수록 대체로 질소 무기화 계수도 큰 경향을 보였다.
질소 무기화 속도상수 k는 토양 유기물 함량 30 g kg-1 이하에서 평균 0.039, 0.036이고, 30 g kg-1 초과에서 평균 0.052 day-1으로 유기물 함량이 많은 토양에서 높은 속도 상수를 보였다. Kim et al. (2005)의 연구결과에서도 토양 유기물 함량이 18 - 42 g kg-1 인 밭토양의 k값을 일 단위로 환산했을 때 0.028 - 0.042 day-1로 유기물 함량이 많은 토양에서 질소 무기화가 빨랐고, 본 연구에서 제시한 k값 범위 내에 해당하였다. 그러나 Shin et al. (2015)은 토양 유기물 함량이 동일한 사질, 식질 토양의 질소 무기화를 구했을 때 k값은 각각 0.125, 0.068 day-1으로 토성에 따라 차이가 있었고, 토양에 투입되는 질소 함량이 동일해도 시용한 유기자재 종류에 따라 k값 차이가 크다고 하였다. 토양 유기물 함량과 질소 무기화 계수가 비례하지 않는 토양의 경우, 유기물의 크기 외에 다른 토양 요인과 질소 무기화 관계를 검토할 필요가 있었다.
밭토양 특성에 따른 질소 무기화 계수 예측
밭토양의 이화학적 특성과 질소 무기화 계수의 상관관계를 구한 결과, 질소 무기화량인 Mineralized N와 N0는 토양 유기물, 총질소와 유의미한 상관이 있었다 (Table 3). 기존 연구결과에 의하면 토양 유기태 질소로 N0를 예측할 수 있고 (Cabrera and Kissel, 1988; Schomberg et al., 2009; Dessureault-Rompré et al., 2010), 유기태 질소를 포함하는 총질소는 잠재적 질소 무기화량을 예측하는 좋은 인자로 활용할 수 있다고 하였다 (Mallory and Griffin, 2007; Dessureault-Rompré et al., 2015). 또한 질소 무기화는 토양 유기물의 크기 및 이분해성 유기물과 1차적으로 연관되어 있으므로 질소 무기화 예측에 의한 비료 추천을 위해서는 유기물의 크기를 반영하는 토양 변수를 고려할 필요가 있었다 (Ros et al., 2011).
Table 3.
The Pearson correlation coefficients among soil nitrogen mineralization factor (Mineralized N, N0 and k) and soil properties (n=40).
|
Sand
|
Clay
|
CEC
|
pH
|
EC
|
SOM
|
T-N
|
C/N
|
|
Mineralized N
|
0.120
|
0.055
|
-0.004
|
0.053
|
0.863***
|
0.505**
|
0.779***
|
-0.071
|
|
N0 |
0.256
|
-0.007
|
0.161
|
0.139
|
0.248
|
0.519**
|
0.453**
|
0.267
|
|
k
|
-0.140
|
0.061
|
-0.083
|
-0.113
|
0.475**
|
0.095
|
0.275
|
-0.322*
|
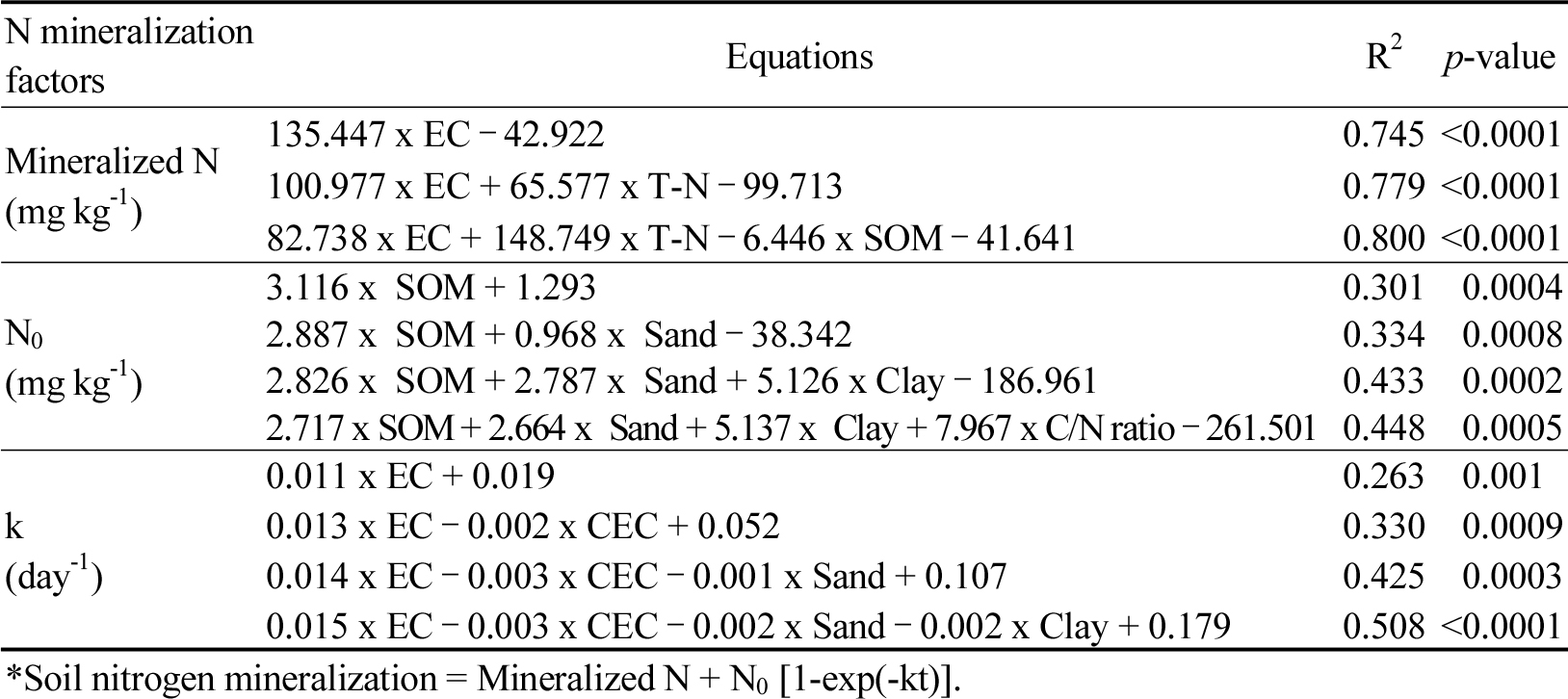
N0의 예측을 위해 Stepwise regression을 수행했을 때 파라미터로 토양 유기물, Sand, Clay, 탄질률이 선정되었으며 (Table 4), 이 중에서 N0와 유의한 상관관계가 있는 파라미터는 토양 유기물이었다. 시험토양의 총질소 함량은 토양 유기물의 0.0682배 (R2=0.729)로 비례 관계가 있어 토양 유기물 함량을 N0 예측을 위한 주요 파라미터로 적용이 가능하다는 것을 확인하였다 (Fig. 1).
Table 4.
Stepwise multiple regression equations relating soil properties to soil nitrogen mineralization factors (Mineralized N, N0 and k) estimated from fitting the first-order kinetic models at 27°C (n=40).
|
Soil N mineralization factors
|
Equations
|
R2 | p-value
|
Mineralized N
(mg kg-1)
|
135.447 x EC ‒ 42.922
|
0.745
|
<0.0001
|
|
100.977 x EC + 65.577 x T-N ‒ 99.713
|
0.779
|
<0.0001
|
|
82.738 x EC + 148.749 x T-N ‒ 6.446 x SOM ‒ 41.641
|
0.800
|
<0.0001
|
N0
(mg kg-1)
|
3.116 x SOM + 1.293
|
0.301
|
0.0004
|
|
2.887 x SOM + 0.968 x Sand ‒ 38.342
|
0.334
|
0.0008
|
|
2.826 x SOM + 2.787 x Sand + 5.126 x Clay ‒ 186.961
|
0.433
|
0.0002
|
|
2.717 x SOM + 2.664 x Sand + 5.137 x Clay + 7.967 x C/N ratio ‒ 261.501
|
0.448
|
0.0005
|
k
(day-1)
|
0.011 x EC + 0.019
|
0.263
|
0.001
|
|
0.013 x EC ‒ 0.002 x CEC + 0.052
|
0.330
|
0.0009
|
|
0.014 x EC ‒ 0.003 x CEC ‒ 0.001 x Sand + 0.107
|
0.425
|
0.0003
|
|
0.015 x EC ‒ 0.003 x CEC ‒ 0.002 x Sand ‒ 0.002 x Clay + 0.179
|
0.508
|
<0.0001
|
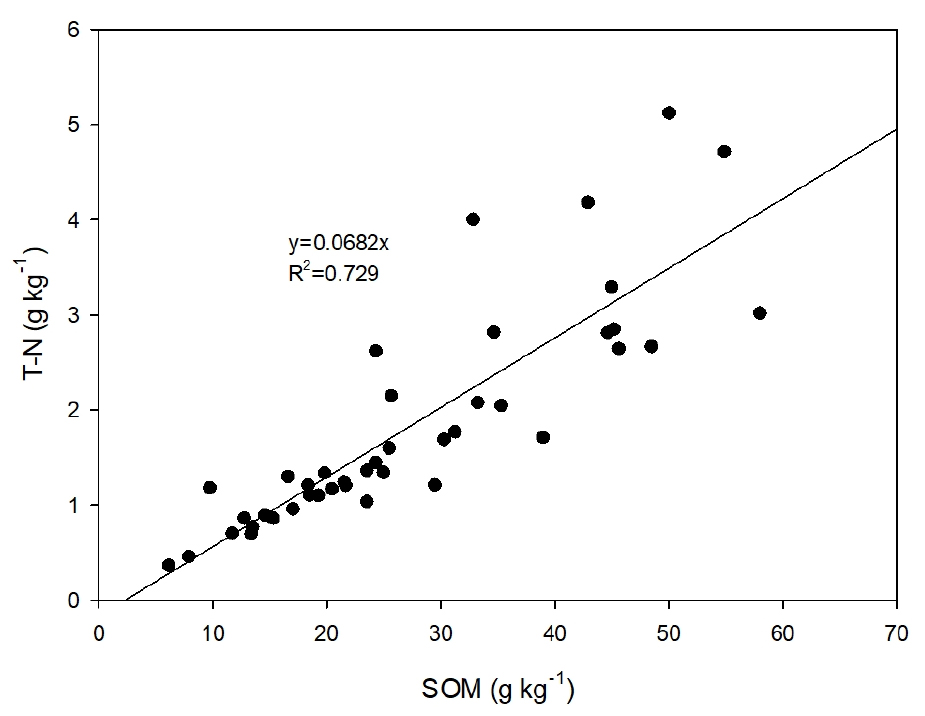
Fig. 1
Relationship between soil organic matter and total nitrogen in the pepper cultivated soils (n=40).
Mineralized N 예측을 위한 파라미터로 EC, 총질소, 유기물 함량이 선정되었다. 토양 중 수용성 이온들을 간접적으로 확인할 수 있는 지표로서 질소 무기화 모니터링에 토양용액의 EC를 활용할 수 있으며 (De Neve et al., 2000; Eigenberg et al., 2002), 본 연구에서도 EC 회귀식으로 Mineralized N의 74.5%를 설명할 수 있었다.
속도상수 k값은 EC와 양의 상관관계, 탄질률과 음의 상관관계가 있었으며, 예측을 위한 회귀식 파라미터로는 EC, CEC, Sand, Clay가 선정되었다. 탄질률은 예측식에서 제외되었는데, Heumann et al. (2003)은 천천히 무기화되는 질소가 많은 밭토양은 탄질률이 낮은 경향이 있었으나, 질소 무기화는 그 외의 요인들이 복합적으로 작용하기 때문에 탄질률이 토양 유기물의 분해 특성과 직접적인 관련이 있다고 보기는 어렵다고 하였다. 본 연구에서도 유기물 함량이 30 g kg-1 이상이고 탄질률이 평균보다 높은 토양에서 k값이 작은 경우가 있었으나, N0값은 300 mg kg-1 이상으로 많아 탄질률이 질소 무기화량에 영향을 미친다고 볼 수는 없었다. k값 예측에 EC가 선정된 것은 초기 무기화량이 급격히 증가할 때 무기화 속도 또한 증가하기 때문에, Mineralized N과 유의한 관계가 있었던 EC가 파라미터로 선정된 것으로 생각된다.
질소 무기화 계수 예측식에 사양토와 식양토인 고추 재배지 토양 이화학성을 적용하여 150일간 질소 무기화량을 비교했을 때, 사양토에서 EC와 질소 무기화량 관계식의 기울기는 135.9, 식양토에서는 152.3 이었고 (Fig. 2), 토양 유기물함량과 질소 무기화량 관계식의 기울기는 사양토에서 9.1466, 식양토에서 9.8615 이었다 (Fig. 3). 유기물함량 30 g kg-1 이하인 토양의 질소 무기화량을 비교해보면 사양토에서 143 mg kg-1이며, 식양토에서 155 mg kg-1 으로 질소 무기화 계수 예측 모델식은 토성에 따른 차이를 반영함을 확인할 수 있었다 (Fig. 3).
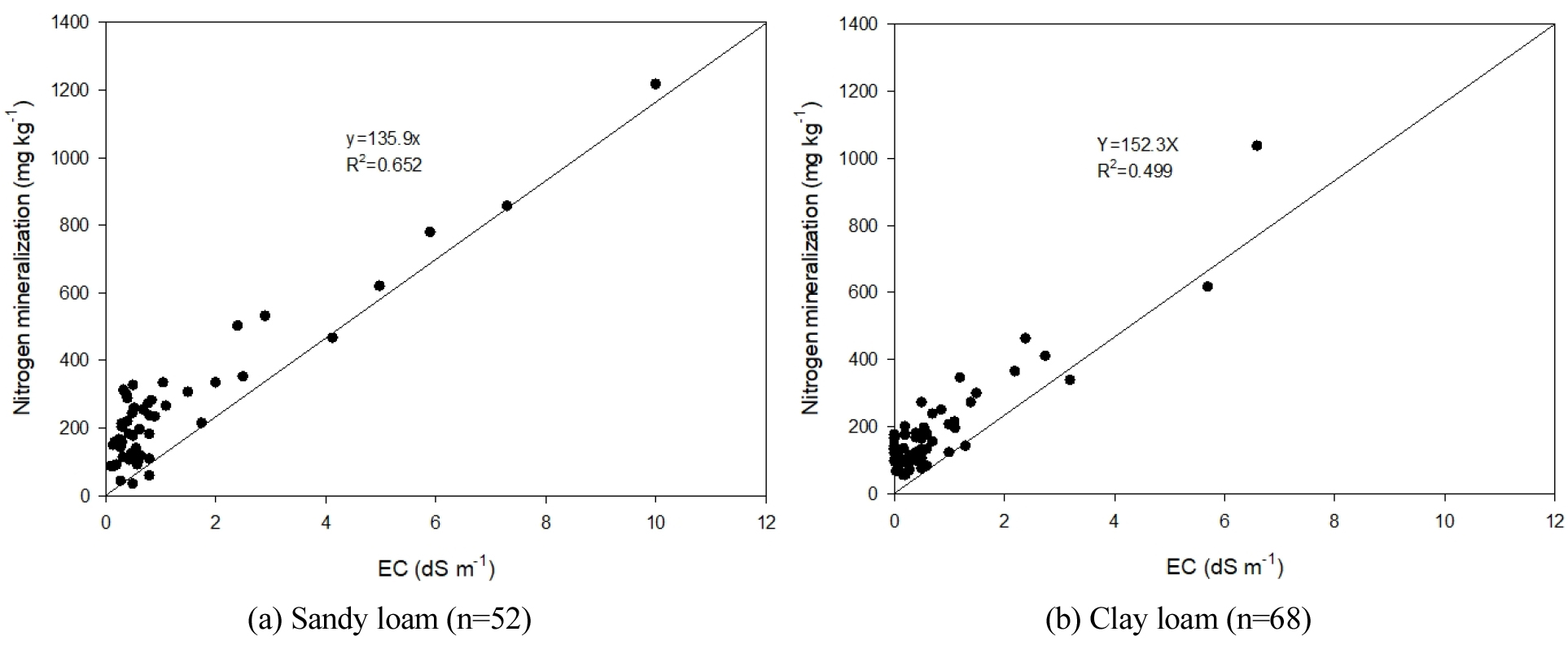
Fig. 2
Relationship between EC and estimated nitrogen mineralization for 150 days in the pepper cultivated sandy loam(a) and clay loam(b) soils.
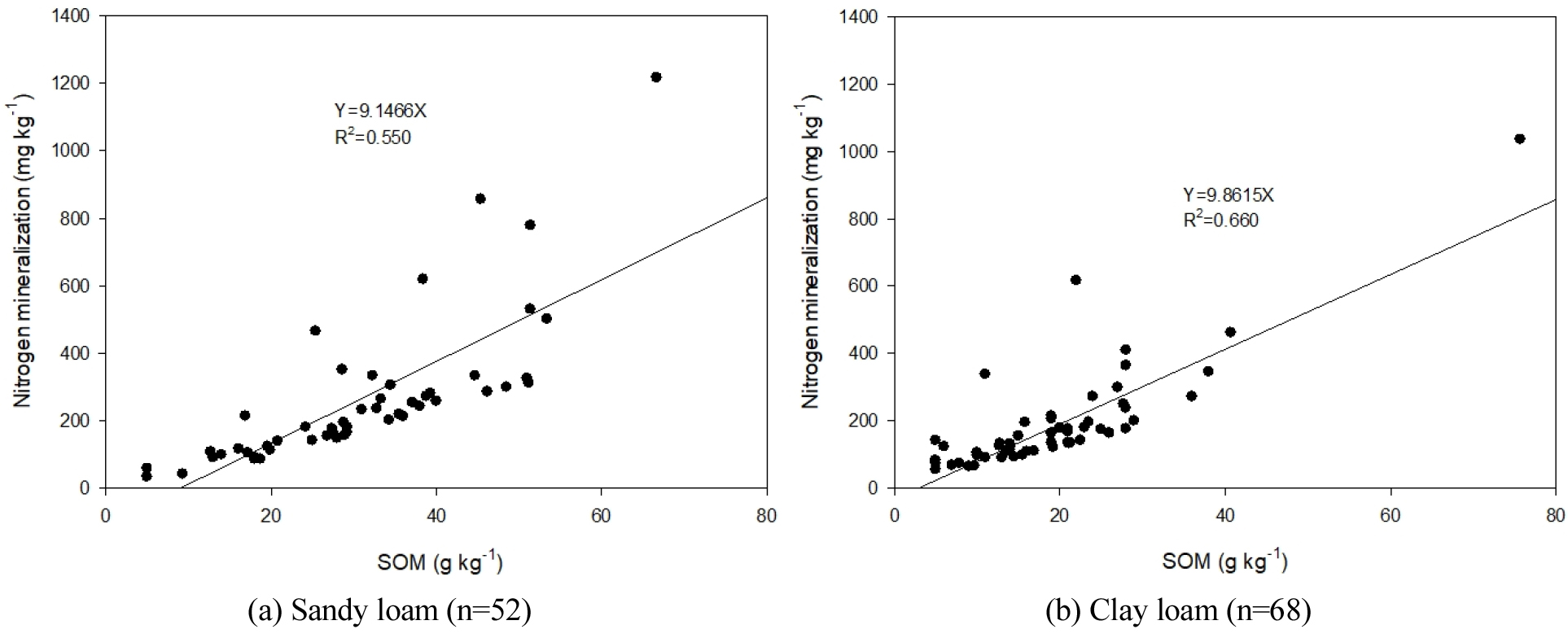
Fig. 3
Relationship between soil organic matter and estimated nitrogen mineralization for 150 days in the pepper cultivated sandy loam(a) and clay loam(b) soils.
Conclusions
결론적으로 질소 무기화량은 토양 유기물, EC, 총질소 등 토양 질소와 직접적으로 관련된 요인들로 예측이 가능하며, 잠재적 질소 무기화량과 무기화 속도 상수 등 질소 무기화 계수를 간접적으로 예측하기 위한 방법으로 Schomberg et al. (2009)과 Dessureault-Rompré et al. (2010)에 의해 제안된 것처럼 토성, 유기물 함량 등 토양 특성을 적용한 모델식을 적용할 수 있음을 확인하였다. 본 연구에서 제안된 몇몇 질소 무기화 계수 추정 모델식의 현장 적용을 위해서는 임의의 밭토양을 대상으로 검증하는 과정이 필요하다.
Acknowledgements
This work was carried out with the support of “Cooperative Research Program for Agriculture Science & Technology Development (Project No. PJ01283701)” Rural Development Administration, Republic of Korea.
References
Bechtold, J.S. and R.J. Naiman. 2006. Soil texture and nitrogen mineralization potential across a riparian toposequence in a semi-arid savanna. Soil Biol. Biochem. 38(6):1325-1333.
10.1016/j.soilbio.2005.09.028Cabrera, M.L. and D.E. Kissel. 1988. Evaluation of a method to predict nitrogen mineralized from soil organic matter under field conditions. Soil Sci. Soc. Am. J. 52(4):1027-1031.
10.2136/sssaj1988.03615995005200040024xCampbell, C.A., B.H. Ellert, and Y.W. Jame. 1993. Nitrogen mineralization potential in soils, p. 341-349. In: M.R. Carter (ed.). Soil sampling and methods of analysis. Lewis Publishers, Boca Raton, FL, USA.
Carpenter-Boggs, L., J.L. Pikul, M.F. Vigil, and W.E. Riedell. 2000. Soil nitrogen mineralization influenced by crop rotation and nitrogen fertilization. Soil Sci. Soc. Am. J. 64(6):2038-2045.
10.2136/sssaj2000.6462038xDe Neve, S., J. Van de Steene, R. Hartmann, and G. Hofman. 2000. Using time domain reflectometry for monitoring mineralization of nitrogen from soil organic matter. Eur. J. Soil Sci. 51(2):295-304.
10.1046/j.1365-2389.2000.00306.xDessureault-Rompré, J., B.J. Zebarth, D.L. Burton, and A. Georgallas. 2015. Predicting soil nitrogen supply from soil properties. Can. J. Soil Sci. 95(1):63-75.
10.4141/cjss-2014-057Dessureault-Rompré, J., B.J. Zebarth, D.L. Burton, M. Sharifi, J. Cooper, C.A. Grant, and C.F. Drury. 2010. Relationships among mineralizable soil nitrogen, soil properties, and climatic indices. Soil Sci. Soc. Am. J. 74(4):1218-1227.
10.2136/sssaj2009.0213Dessureault-Rompré, J., B.J. Zebarth, T.L. Chow, D.L. Burton, M. Sharifi, A. Georgallas, and C.A. Grant. 2011. Prediction of soil nitrogen supply in potato fields in a cool humid climate. Soil Sci. Soc. Am. J. 75(2):626-637.
10.2136/sssaj2010.0305Eigenberg, R.A., J.W. Doran, J.A. Nienaber, R.B. Ferguson, and B.L. Woodbury. 2002. Electrical conductivity monitoring of soil condition and available N with animal manure and a cover crop. Agri. Ecosys. Environ. 88(2):183-193.
10.1016/S0167-8809(01)00256-0Gee, G.W. and J.W. Bauder. 1986. Particle size analysis. Methods of soil analysis. part1, p. 383-411. In: A. Klute (ed.), Am. Soc. Agron., Madison, WS, USA.
10.2136/sssabookser5.1.2ed.c15Gilmour, C.M., F.E. Broadbent, and S.M. Beck. 1977. Recycling of carbon and nitrogen through land disposal of various wastes. p. 178-179. In: L.F. Elliott (ed.). Soils for management of organic wastes and waste waters. SSSA, ASA, CSSA, Madison, WS, USA.
Heumann, S., J. Böttcher, and G. Springob. 2002. N mineralization parameters of sandy arable soils. J. Plant Nutr. Soil Sci. 165(4):441-450.
10.1002/1522-2624(200208)165:4<441::AID-JPLN441>3.0.CO;2-FHeumann, S., J. Böttcher, and G. Springob. 2003. Pedotransfer functions for the pool size of slowly mineralizable organic N in sandy arable soils. J. Plant Nutr. Soil Sci. 166:308-318.
10.1002/jpln.200390048Kim, S.H., H.Y. Hwang, M.S. Kim, S.J. Park, J.H. Shim, and Y.H. Lee. 2020. Assessment of fertilizer usage by food crops at the national level. Korean J. Soil. Sci. Fert. 53(2):231-236.
Kim, Y.H., S.K. Kim, and Y.S. Zhang. 2005. Determination of soil nitrogen supplying capacity using pepsin digestibility. Korean J. Soil Sci. Fert. 38(5):253-258.
Lee, Y.J., S.B. Lee, Y.M. Kim, Y.S. Song, and D.B. Lee. 2019. Relation of Organic Matter Content and Nitrogen Mineralization of Soils Collected from Pepper Cultivated Land. Korean J. Environ. Agric. 38(3):119-123.
10.5338/KJEA.2019.38.3.26Mallory, E.B. and T.S. Griffin. 2007. Impacts of soil amendment history on nitrogen availability from manure and fertilizer. Soil Sci. Soc. Am. J. 71(3):964-973.
10.2136/sssaj2006.0244Rasmussen, P.E., C.L. Douglas Jr., H.P. Collins, and S.L. Albrecht. 1998. Long-term cropping system effects on mineralizable nitrogen in soil. Soil Biol. Biochem. 30(13):1829-1837.
10.1016/S0038-0717(98)00057-1RDA (Rural Development Administration). 2017. Annual report of the monitoring project on agro-environmental quality. RDA, Wanju, Korea.
Reddy, K.R., R. Khaleel, M.R. Overcash, and P.W. Westerman. 1979. A nonpoint source model for land areas receiving animal wastes: I. Mineralization of organic nitrogen. Trans. Am. Soc. Agric. Eng. 22(4):863-0872.
10.13031/2013.35116Ros, G.H., M.C. Hanegraaf, E. Hoffland, and W.H. van Riemsdijk. 2011. Predicting soil N mineralization: Relevance of organic matter fractions and soil properties. Soil Biol. Biochem. 43(8):1714-1722.
10.1016/j.soilbio.2011.04.017Schomberg, H.H., S. Wietholter, T.S. Griffin, D.W. Reeves, M.L. Cabrera, D.S. Fisher, and N.R. Kitchen. 2009. Assessing indices for predicting potential nitrogen mineralization in soils under different management systems. Soil Sci. Soc. Am. J. 73(5):1575-1586.
10.2136/sssaj2008.0303Sharifi, M., B.J. Zebarth, D.L. Burton, C.A. Grant, G.A. Porter, J.M. Cooper, and W. J. Arsenault. 2007. Evaluation of laboratory-based measures of soil mineral nitrogen and potentially mineralizable nitrogen as predictors of field-based indices of soil nitrogen supply in potato production. Plant Soil. 301(1-2):203-214.
10.1007/s11104-007-9438-7Shin, J.H., S.M. Lee, and B.W. Lee. 2015. Estimation of N Mineralization Potential and N Mineralization Rate of Organic Amendments in Upland Soil. Korean J. Soil Sci. Fert. 48(6):751-760.
10.7745/KJSSF.2015.48.6.751Stanford, G. and S.J. Smith. 1972. Nitrogen mineralization potentials of soils. Soil Sci. Soc. Am. J. 36(3):465-472.
10.2136/sssaj1972.03615995003600030029xYun, H.B., C.Y. Yu, J.E. Yang, S.M. Lee, J.H. Shin, S.C. Kim, and Y.B. Lee. 2010. Soil Nitrogen Mineralization Influenced by Continuous Application of Livestock Manure Composts. Korean J. Soil Sci. Fert. 43(3):329-334.