Introduction
전 세계적으로 가축 사육 수가 증가함에 따라 가축의 질병 예방 및 치료, 그리고 성장 촉진 등을 위해 항생제 소비량이 증가하고 있다 (Yao et al., 2017). 선행 연구에 따르면 2030년까지 전 세계 항생제의 소비가 2010년과 비교하여 약 67% 정도 증가할 수 있다는 예측 보고가 있으며 (Van Boeckel et al., 2015) 국내의 경우 가축에 사용되는 항생제가 2009년부터 2018년까지 평균 950톤 (820 - 1,046톤) 가량 소비되었다 (Seo et al., 2018a, 2018b).
항생제의 오남용은 항생제 저항 유전자 (Antibiotic resistance genes)를 생성할 수 있으며 특히 농업환경에서는 체외로 배출된 항생제가 환경 중에 잔류할 수 있는 확률이 높아진다 (Awad et al., 2015; Kim et al., 2019). 가축에게 투여된 항생제는 가축의 체내에서 10 - 20% 정도만이 사용되고 나머지는 체외로 배출되는 특성이 있다 (Hong et al., 2019; Jjemba, 2002).
체외로 배출된 항생제는 주로 분뇨에 잔류하며 농업환경에서 작물의 공급 및 토양질 개선 등을 위해 분뇨는 퇴비화 되어 농경지에 사용된다 (Larney et al., 2006). 이 과정에서 퇴비에 잔류하는 항생제가 토양에 유입되며 강우에 의해 지하수 또는 지표수로 유입되어 잔류하게 된다 (Kummerer, 2009; Qiao et al., 2012; Boy-Roura et al., 2018). 또한 농경지에 잔류한 항생제는 작물 재배 시 작물체로 전이하여 작물체 내에 축적되거나 생장을 억제 하기도 한다 (Kong et al., 2007; Hillis et al., 2011; Pan and Chu, 2016, 2017).
농업 환경에 잔류하는 항생제의 농도는 항생제 종류 및 지역별 특성에 따라 매우 상이하다. 네덜란드의 가축 농장 지역 지하수를 대상으로 잔류 항생제를 분석한 결과 sulfamethazine는 0.3 - 12.5 ng L-1의 범위로 22개 항생물질 중 가장 많은 지역에서 검출되었고, sulfamethoxazole의 경우 최대 18 ng L-1까지 검출되었다 (Kivits et al., 2018). 중국의 경우 축사 주변 환경에서 잔류 항생제에 대한 모니터링 결과 분뇨와 토양에서 각각 최대 143.97 mg kg-1, 1,590.16 µg kg-1의 chlortetracycline을 검출하였다 (An et al., 2015). 국내의 경우 농업 환경 중 토양과 저니토에서 각각 sulfamethazine (2.34 - 3.02 µg kg-1), tetracycline (1.02 - 10.11 µg kg-1), chlortetracycline (1.02 - 21.35 µg kg-1) 등이 검출되었고 (Kim et al., 2017), 지하수에서 sulfamethazine (26.6 - 40.0 ng L-1)이 검출되었다 (Hong et al., 2019).
본 연구의 목적은 농업 환경에 잔류하는 항생제의 잔류 농도를 모니터링 하기 위해 가축 농장 인근 농경지 토양과 하천수 및 저니토 내 잔류 항생제를 모니터링하고 토양의 이화학적 특성 중 항생제의 잔류 특성에 영향을 미치는 인자를 규명하고자 하였다.
Materials and Methods
Chemicals 본 시험에서는 테트라사이클라인 (Tetracycline, TCs) 계열 항생제 3종류, 테트라사이클라인 (TC), 클로르테트라사이클라인 (CTC), 옥시테트라사이클라인 (OTC)과 설폰아마이드 (sulfonamide, SAs) 계열 항생제 3종류, 설파메타진 (SMT), 설파메토자졸 (SMX), 설파티아졸 (STZ)을 대상으로 모니터링을 실시하였다. 각 항생제의 표준품 (stock)은 순도가 90 - 99% 인 분말 형태의 시약을 사용하였으며 표준 용액 (standard solution)은 표준품 10 mg을 10 mL의 메탄올 (MeOH)에 용해시켜 1,000 mg L-1의 농도로 제조한 후 증류수에 희석하여 실험에 사용하였다. 모든 표준 용액은 4°C 에서 냉장 보관하였다.
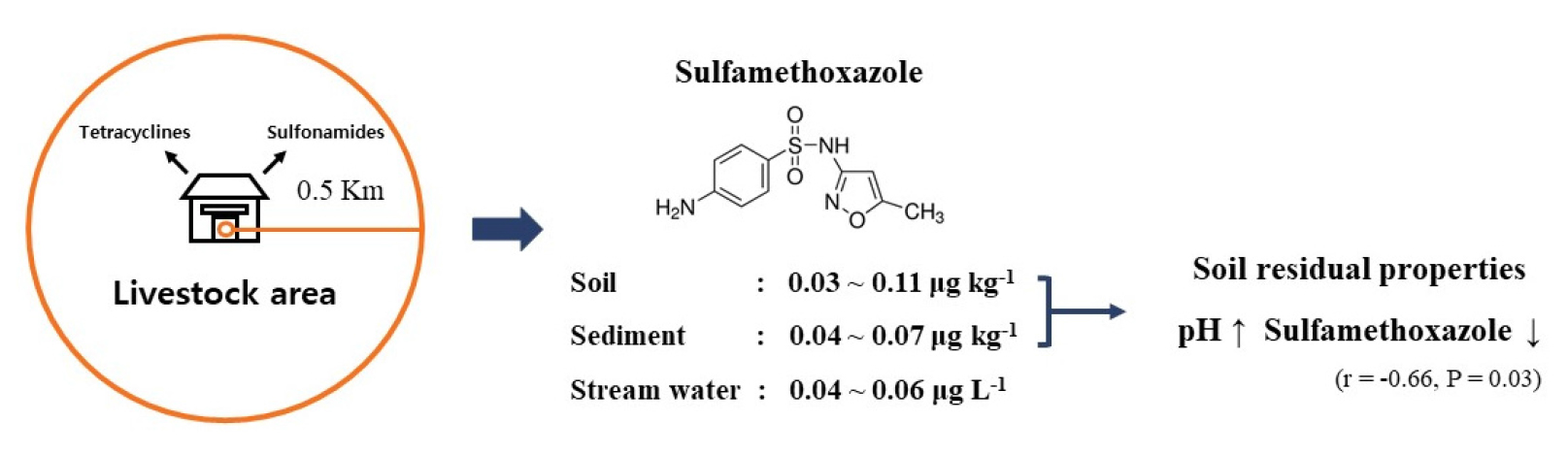
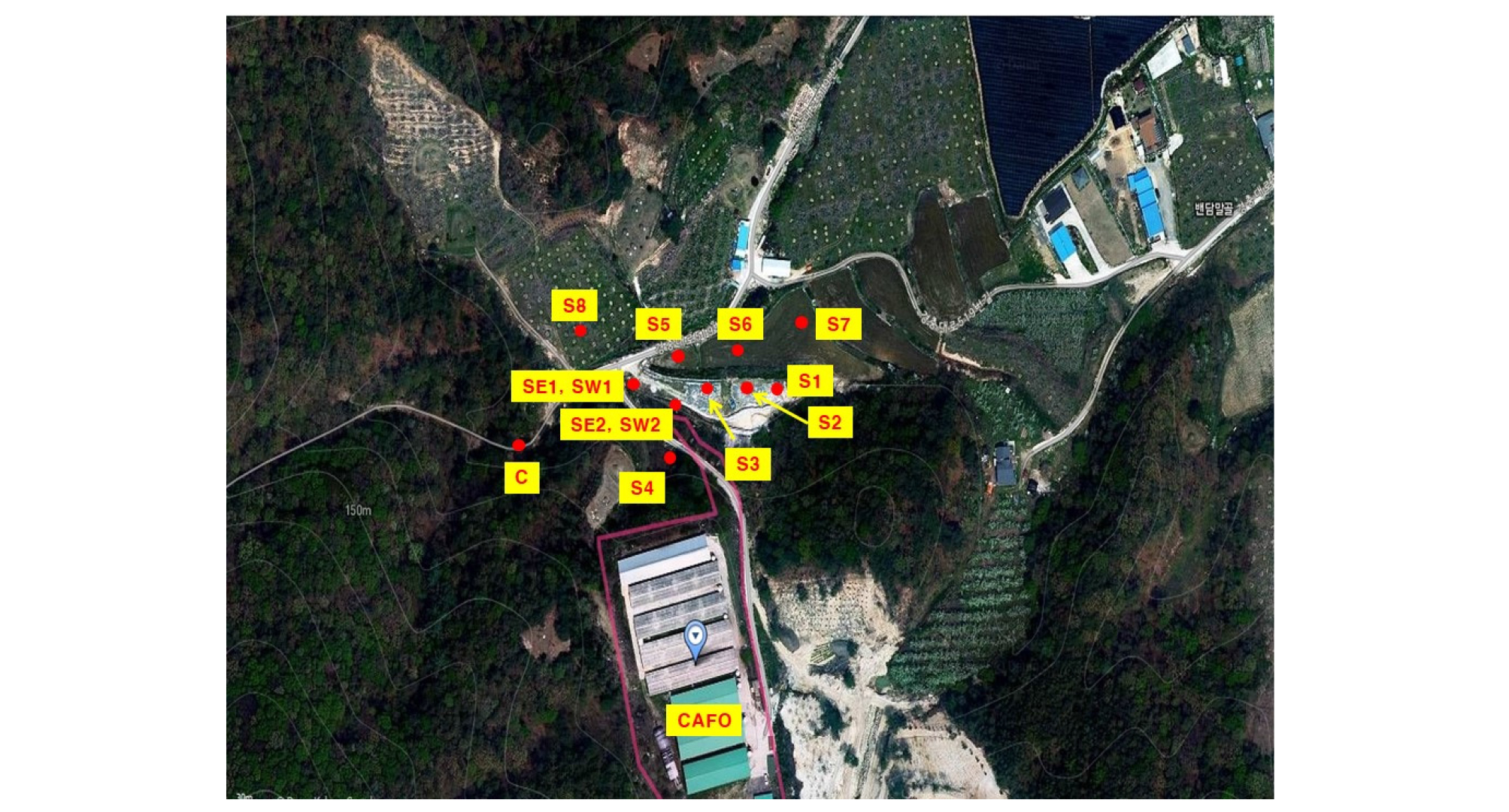
Sample collection 농촌 지역의 항생제 잔류 농도를 모니터링 하기 위해 경기 지역에 위치한 가축 농장을 중심으로 반경 0.5 Km 이내 주변 농경지 토양 8 지점, 저니토 2지점, 그리고 하천수 2 지점을 선별하였으며 대조구는 산림 토양을 채취하였다 (Fig. 1). 각 시료 지점에 대한 설명은 Table 1에 정리하였다. 토양 시료는 휴대용 토양 채취기를 이용하여 표토 (0 - 15 cm)를 채취하였으며 각 시료 채취 지점당 3 - 5개의 시료를 채취한 후 하나의 시료로 합쳐 대표 시료를 만들었다. 하천수 시료는 샘플 용기를 하천수로 2 - 3회 세척한 후 기포가 생기지 않도록 채수병을 가득 채워 시료를 채취하였다. 저니토 시료는 하천수 시료를 채취한 동일 지점에서 채취하였으며 휴대용 시료 채취기를 이용하여 주변 저니토 2 - 3지점의 시료를 하나로 합쳐 대표 시료를 만들었다.
Table 1.
Site description and chemical properties of samples.
채취된 시료는 얼음이 채워진 아이스박스에 옮겨 실험실로 운반한 후 토양과 저니토 시료는 암조건에서 풍건 하였으며 풍건된 시료는 2 mm로 체거름하여 상온 (20°C)에서 보관하였다. 하천수 시료는 0.45 µm 공극 크기의 여과지로 여과한 후 4°C에서 냉장보관 하였다.
Chemical analysis 토양과 저니토의 화학적 특성 분석은 국립농업과학원의 토양 및 식물체 분석법을 참조하였으며 하천수의 화학적 특성 분석은 수질오염공정시험법 (MOE, 2004)을 참조하였다. 토양과 저니토의 pH와 전기전도도 (EC)는 각각 pH (MP 220 Mettler Toledo, USA)와 EC meter (Mettler Toledo, S230, USA)를 사용하여 측정하였다. 유기물 함량과 유효인산 농도는 각각 Walkley Black 방법과 Bray No.1 방법을 이용하여 전처리 후 UV/vis spectrometry (UV 240, Schimadzu, Japan)의 610, 660 nm 파장에서 비색 정량 하였다. 토양과 저니토의 NO3-N 농도는 습토 10 g을 2M KCl 50 mL로 30분간 진탕한 후 Whatman No. 2 여과지로 여과한 후 자동원소분석기 (Thermo Fisher, Gallery, USA)를 이용하여 측정하였다 (Lee et al., 2017). 하천수의 pH, EC, NO3-N은 모두 동일 기기를 사용하여 측정하였다.
Sample preparation and solid phase extraction (SPE) 토양, 저니토, 및 하천수 내 잔류 항생제 분석을 위한 전처리 과정과 고형상 추출법 (SPE) 방법은 선행 연구를 참조하였다 (Kim et al., 2019). 토양 및 저니토 시료 1 g을 튜브에 넣고 Mcllvaine 완충 용액을 이용하여 2번 추출한 후 총 40 mL의 추출제에 증류수를 혼합하여 총 120 mL이 되도록 한 후 0.45 µm 공극의 여과지를 이용하여 감압 추출 하였다.
하천수의 경우 시료 120 mL를 250 mL 삼각플라스크에 넣고 40% (v/v)로 희석한 황산 (H2SO4) 용액을 이용하여 시료의 pH를 2.5 - 3.0으로 조절하였다. 그 후 5% Na2EDTA (w/v) 0.5 mL를 넣고 15분 동안 150 rpm에서 교반 하였다.
전처리된 토양 및 저니토 시료와 교반된 하천수 시료는 manifold (Visiprep, Supelco, USA)를 이용하여 고형상 추출 (SPE)을 시행하였다. 고형상 추출에 사용된 카트리지는 Oasis HLB (3cc/60 mg, Waters, USA) 였으며 시료를 포집 하기 전 메탄올 (MeOH), 0.5N (v/v) 염산용액, 증류수를 각각 3 mL씩 순차적으로 카트리지에 흘려주어 카트리지를 활성화 시켰다. 시료의 포집 속도는 3 mL min-1 정도로 유지하였으며 포집이 끝난 후에는 증류수를 이용하여 3 mL씩 3회 (총 9 mL) 세척하였다.
카트리지에 포집된 항생제를 추출하기 위해 15 mL 튜브 (conical bottom centrifuge tube)에 내부표준물질 (internal standard)인 simeton (0.24 mg L-1) 0.05 mL를 넣고 메탄올 5 mL로 용리 (elution)하였다. 용리된 시료는 질소농축기 (N-Evap-11. OASYS, USA)에서 50°C 항온 조건을 유지하여 50 µL까지 농축 후 70 µL의 이동상 용액 (mobile phase A, 0.1% formic acid + 99.9% HPLC water)을 넣고 진동 혼합 후 기기 분석에 사용하였다.
HPLC/MS/MS analysis 항생제 정량을 위한 분석 기기는 액체 크로마토그래피 (Agilent 1200, USA)와 질량 분석기 (API, 6000 Q TRAP, ABSCIEX, Canada)를 사용하였으며 컬럼은 공극 크기가 3.5 µm이며, 내경이 4.6mm인 ZORBAX Eclipse Plus C18 컬럼을 사용하였다. 이동상 (Mobile phase) A는 99.9% D.I water + 0.1% formic acid, B는 99.9% acetonitrile + 0.1% formic acid를 사용하였으며 유속은 0.7 mL min-1으로 조절하였다. 내부 표준 물질과 6종류의 항생제는 다성분 분석을 통해 동시 분석하였으며 총 분석 시간은 15분이 소요되었다.
QA/QC and statistical analysis 항생제 정량을 위한 분석 조건의 정도 관리 (QA/QC)를 위해 회수율 (recovery)과 정량 한계 (LOD, Limit of Quantification)를 산출하였다. 회수율 검증과 정량 한계 산출 방법은 선행 연구 (Kim et al., 2019)를 참조하였다. 모든 분석 결과는 3반복 실험 결과의 평균값을 이용하였으며 유의성 검정을 위해 유의수준 95% 수준 (p < 0.05)에서 ANOVA 분석을 실시하여 각 결과값의 유의성을 검증하였다.
Results and Discussion
Chemical properties of groundwater 토양, 저니토, 및 하천수의 화학적 특성은 Table 1에 정리하였다. 토양의 pH는 4.90 - 8.42의 범위를 나타냈으며 논 토양의 pH (4.90 - 5.95)가 밭 토양 (6.55 - 8.42) 또는 과수원 토양 (6.41)의 pH에 비해 낮게 조사되었다. 국내 논 토양의 평균 pH는 5.5 - 6.5 범위를 나타내며 밭 토양 및 과수원토양의 평균 pH는 6.5 - 7.5의 범위를 나타내어 조사 지점의 토양 pH는 국내 농경지 토양의 평균 범위에 포함되었다 (Choi et al., 2018). 전기전도도 역시 논 토양의 EC (0.14 - 0.28 dS m-1)가 밭 토양 (0.40 - 0.73 dS m-1)과 과수원 토양 (0.57 dS m-1)의 EC 값에 비해 낮았다. 논 토양의 pH와 EC는 담수 여부에 따라 변화가 나타나며 담수 조건에서 산성토양의 경우 토양 pH가 상승하는 경향이 있는 반면 비담수 조건에서는 토양 pH가 낮아지는 경향이 있다. 시료 채취 시기가 비담수 기간 (3월)인 점을 고려하였을 경우 논 토양의 pH가 밭 토양 또는 과수원 토양에 비해 낮은 경향을 나타내었다.
토양의 유기물 함량과 유효 인산의 농도는 각각 10.4 - 67.6 g kg-1, 91.2 - 263.0 mg kg-1의 범위로 조사되었다. 국내 농경지 토양의 적정 유기물 함량은 20 - 35 g kg-1 이며 유효 인산 농도의 경우 논 토양 (80 - 120 mg kg-1), 밭 토양과 과수원 토양 (300 - 550 mg kg-1)을 감안할 경우 조사 지역의 유기물 함량은 S1과 S3 지점을 제외하고는 적정 범위에 비해 높은 함량을 가지고 있었으며 유효 인산의 경우 논토양에서는 적정범위보다 높은 농도의 유효 인산 농도가 함유되었으나 밭토야에서는 적정 범위에 비해 낮은 함량의 유효 인산이 포함된 것으로 조사되었다.
Recovery and limit of quantification of antibiotics 토양, 저니토, 그리고 하천수의 잔류 항생제 정량을 위한 분석 조건의 회수율과 정량 한계는 Table 2에 정리하였다. 총 6 종류의 항생제에 대한 정량 곡선은 0.01 - 5.00 mg L-1 범위에서 산정하였고 R2 값은 6 종류 모두 0.98 - 0.99로 계산되었다. 각 항생제의 회수율은 하천수 (89 - 112%), 토양 (72 - 90%), 저니토 (72 - 86%) 범위에서 산출되었으며 정량 한계는 하천수 (0.02 µg L-1), 토양과 저니토 (0.02 - 0.25 (µg kg-1)로 산출 되었다.
Table 2.
Summary of QA and QC for quantification of antibiotics (n=3).
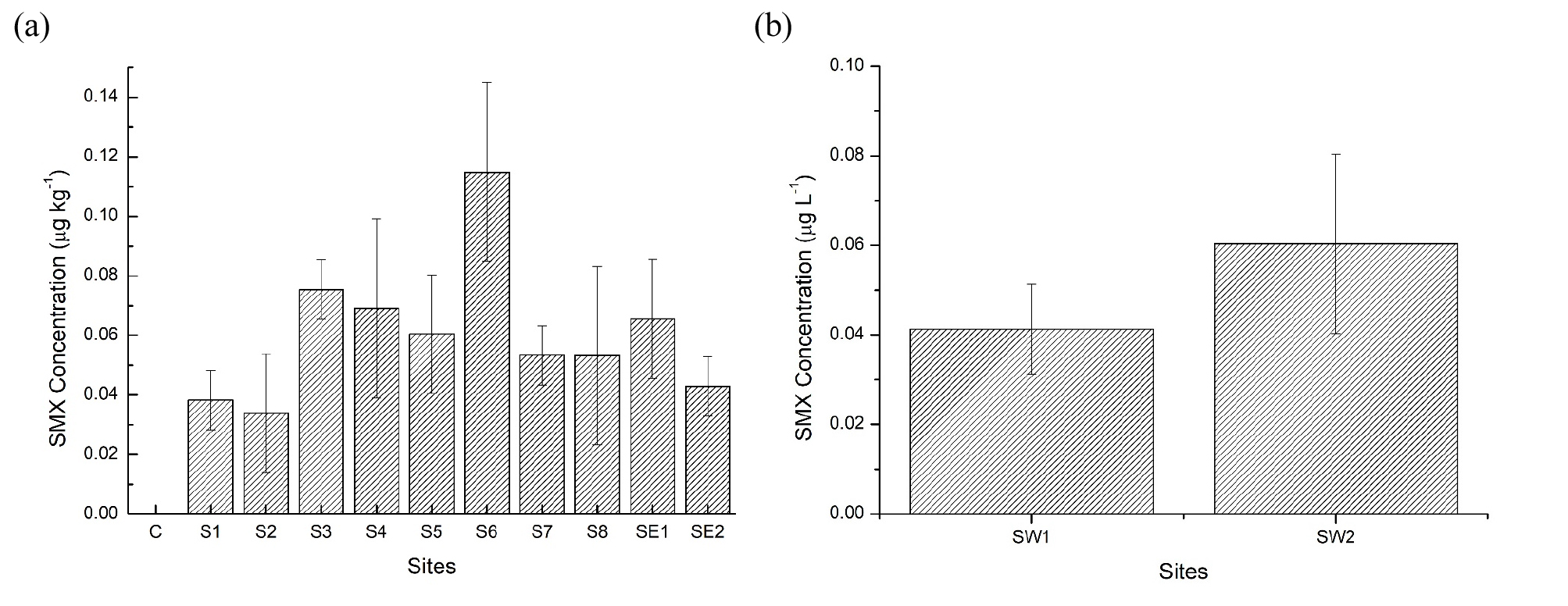
Occurrence of veterinary antibiotics 농촌 지역 가축 농장을 중심으로 인근 토양 및 저니토와 지표수 내의 잔류 항생제 농도는 Fig. 2에 정리하였다. 총 6 종류의 항생제 중 SMX만이 모든 토양 및 저니토와 지표수에서 검출 되었다. 토양의 경우 SMX의 검출 농도는 0.03 - 0.11 µg kg-1의 범위였으며 저니토에서의 SMX 검출 농도는 0.04 - 0.07 µg kg-1, 그리고 하천수에서의 SMX 검출 농도는 0.04 - 0.06 µg kg-1 수준이었다. 가축 농장을 기준으로 가장 아래 지점에 위치해 있는 S6 지점의 토양 내 SMX 농도가 0.11 µg kg-1로 가장 높았으며 S1, S2 지점의 SMX 농도가 0.04, 0.03 µg kg-1로 가장 낮았다.
설폰아마이드 계열의 항생제는 약산성의 극성 (polar)을 나타내며 물에 잘 녹고 Kow (물-유기용매 분배 계수)의 값 (log Kow: -0.1-1.7)이 낮아 주변 하천수 또는 지하수로 유입 가능성이 높은 계열의 항생제 이다 (Wang and Wang, 2015; Chen et al., 2017; Chen and Xie, 2018). 국내 농촌 지역의 토양 내 잔류 항생제 농도를 보면 SAs의 경우 0.12 - 3.22 µg kg-1의 범위에서 검출되었으며 SMX와 STZ의 검출 빈도가 가장 높았다 (Kim et al., 2019). 국외의 경우 설파메타진 (SMT)의 토양 내 잔류 농도가 ND (not detected) - 110 µg kg-1의 범위에서 검출되었으며 (Ostermann et al., 2014) Garcia-Galan et al. (2013)의 연구에 의하면 총 16 종류 SAs의 토양 내 검출 농도를 모니터링 결과 총 17개 지점의 샘플 중에서 47%인 8개의 샘플에서 SAs가 검출 되었고 평균 검출 농도는 0.11 - 8.53 µg kg-1의 범위로 조사되었다 (Garcia-Galan et al., 2013). 국내외 농업 환경에서의 SAs 항생제 검출 분포 결과를 비교하였을 경우 지역별 특성에 따라 검출 농도는 상이 하였으며 이는 지역에 따른 사용되는 항생제의 종류, 항생제의 환경 유출 경로, 그리고 항생제의 환경 내 거동 특성에 따라 다를 수 있다는 점을 나타낸다.
Correlation between chemical properties and veterinary antibiotics in the groundwater 토양의 화학적 특성과 SMX의 상관 관계는 Table 3에 정리하였다. SMX의 토양 내 잔류 특성과 상관 관계가 가장 높은 화학적 특성은 토양 pH로 역의 상관 관계 (-0.66)를 나타냈으며 95% 신뢰 수준 (p-value = 0.03)에서 통계적으로 유의 하였다. 항생제는 토양의 pH에 따라 양이온, zwitter 이온, 그리고 음이온으로 존재가 가능하다 (Wang and Wang, 2015). SAs 계열의 항생제 경우 2개의 pKa (pKa1 : 1.7, pKa2 : 5.6)를 가지고 있으며 토양의 pH에 따라 SAs의 존재 형태가 달라지고 이에 따른 흡착 특성이 달라진다.
Table 3.
Correlation analysis between chemical properties of soil and SMX.
| pH | EC | OM | P2O5 | NO3-N | SMX | |
| pH | 1.00 | |||||
| EC | 0.51 | 1.00 | ||||
| OM | -0.54 | 0.15 | 1.00 | |||
| PM2O5 | -0.61 | 0.14 | 0.81** | 1.00 | ||
| NO3-N | 0.35 | -0.29 | -0.57 | -0.81** | 1.00 | |
| SMX | -0.66* | -0.41 | 0.19 | 0.37 | -0.09 | 1.00 |
** Denotes that correlation was significantly different at p < 0.01.
토양의 pH가 5.6 이상인 경우 SAs는 음이온의 형태로 존재하며 토양의 pH가 1.7과 5.6 사이 에서는 중성의 형태로 존재한다 (Chen et al., 2017). 따라서 토양의 pH가 증가함에 따라 SAs의 흡착은 감소하게 된다 (Wang and Wang, 2015; Park and Huwe, 2016).
토양 내 유기물 함량 또한 항생제의 토양 잔류 특성에 영향을 나타낸다. SAs 계열의 항생제는 아닐린 (aniline) 그룹과 아마이드 (amide) 그룹의 작용기를 포함하고 있다. 두 그룹의 작용기는 토양에 흡착하는 특성이 높지 않으며 SAs와 유기물의 흡착은 SAs 계열에 함유되어 있는 알킬 그룹 (R-SAs)과 유기물의 양이온 교환 (cationic exchange) 메커니즘으로 주로 발생한다 (Gao and Pedersen, 2005). SMX의 경우 토양 내 흡착 계수 (Kd)가 4.61 - 2,383.3 L kg-1의 넓은 범위를 나타내며 이는 토양 내 용존 탄소 (DOC, Dissolved Organic Carbon) 함량과 상관 관계가 있어 용존 탄소 함량이 높을수록 SMX의 토양 흡착 계수는 증가 하였다 (Chen et al., 2017).
하지만 본 연구에서는 토양 내 유기물 함량과 SMX의 상관 계수가 0.19로 통계적으로 유의한 상관 관계 (p-value = 0.59)는 없었지만 양의 상관 관계를 나타내어 유기물 함량이 증가할수록 SMX의 잔류 확률도 증가하였다는 것을 알 수 있었다.
Conclusions
농촌 지역의 가축 농장을 중심으로 토양, 저니토, 그리고 하천수에서의 잔류 항생제를 모니터링 하였다. 총 6종류의 TCs와 SAs 항생제 중 SMX 만이 토양, 저니토, 하천수에서 검출 되었다. SMX의 검출 농도는 토양 (0.03 - 0.11 µg kg-1), 저니토 (0.04 - 0.07 µg kg-1), 그리고 하천수 (0.04 - 0.06 µg kg-1) 였으며 가축 농장과의 거리적 상관성은 없었다. 토양의 화학적 특성과 SMX의 잔류 농도에 대한 상관 관계 분석 결과 토양 pH가 SMX의 잔류 농도와 통계적으로 유의한 음의 상관 관계 (-0.66, p-value = 0.03)를 나타내어 토양의 pH가 증가할수록 SMX의 잔류 농도는 감소함을 알 수 있었다. 이는 SMX의 pKa 값에 따라 토양 pH가 pKa2 값보다 높을 경우 SMX는 음이온의 형태로 환경에 잔류하게 되고 토양 pH가 높아짐에 따라 전기 인력적 반발력에 의해 SMX의 토양 흡착이 감소하게 되어 SMX의 잔류 농도는 감소하였다.