Introduction
일반적으로 식물의 생장은 많은 비생물학적 및 생물학적 요인들에 의해 영향을 받는다. 식물의 뿌리 주변 영역인 토양 근권의 환경 조건이 식물 생장에 중요한 역할을 하며, 이들 많은 인자들 중에서 특히 토양 미생물 활동의 영향을 많이 받는 것으로 알려져 있다 (Bloemberg and Lugtenberg, 2001).
식물 생장 촉진 미생물 (plant growth-promoting rhizobateria: PGPR)은 뿌리 및 줄기를 식민지화하고 뿌리 성장에 도움이 되는 자유 생활 미생물이며 많은 종류의 식물 근권에 존재하면서 식물에 유익한 생장 촉진 효과를 나타낸다. 이들 많은 종류의 PGPR은 인돌아세트산 (IAA) 혹은 지베렐린 (GA)등의 식물 생장 호르몬 생성, 무기 인산염 등의 가용화, 질소고정 (nitrogen fixation), 철 킬레이트 siderophore를 통한 철분 영양 증가 및 휘발성 화합물 생성 등의 기작으로 식물 성장에 직접적인 영향을 미친다. 또한 항생제, 공간 및 영양소 경쟁, 뿌리 및 잎 병원체 균주의 광범위한 스펙트럼에 대한 식물의 전신 저항 유도에 의해 PGPR은 뿌리 병원체 및 뿌리 줄기의 다른 유해한 미생물의 개체수를 감소시켜 식물 성장에 도움이 되는 것으로 알려져 있다. 토양에 존재하는 많은 미생물들이 식물 생장 촉진 미생물 (PGPR)로 알려지고 있으며 특히 Pseudomonas, Azospirillum, Burkholderia, Bacillus 및 Serratia 등의 다양한 미생물들이 식물 생장을 촉진시키는 것으로 잘 알려져 있다 (Glick 1995; Jeon et al., 2003; Vessey, 2003; Dey et al., 2004; Lugtenberg and Kamilova, 2009; Bhattacharyya and Jha, 2012; Bal et al., 2013; Islam et al., 2016; Backer et al., 2018).
식물 무기 영양소 중에서 인산 (Phosphorus: P)은 질소 (nitrogen: N) 다음으로 중요한 식물의 핵심 필수 영양소이면서 호흡 및 콩과 식물에서의 질소 고정 작용, 식물의 광합성 작용등 식물의 생장에 필요한 주요 대사 과정에서 중요한 기능을 담당하고 있다 (Saber et al., 2005). 일반적으로 토양에서의 인산은 무기 또는 유기 형태로 풍부하게 존재하고 있지만 대부분 식물이 흡수할 수 없는 불용성 형태로 존재하며 따라서 식물 생장의 주요 생장 제한 인자로 작용하고 있다 (Rengel and Marschner, 2005). 특히 인산 가용화 미생물 (phosphate solubilizing bacteria: PSM)은 토양 내에서 불용성 형태의 인산 화합물을 가용성 형태로 전환시키는데 중요한 역할을 하며 지금까지 많은 인산 가용화 미생물들이 보고 되고 있다. 또한 현재까지 알려진 많은 인산 가용화 미생물들은 인산 가용화 활성 능력뿐만 아니라, 식물 생장 호르몬 생성등 다양한 기능을 가지면서 식물 생장을 촉진시키는 효과를 나타내는 것으로 알려져 있다 (Illmer and Schinner, 1992; Rodriguez and Fraga, 1999; Khan et al., 2009; Lugtenberg and Kamilova, 2009; Sharma et al., 2013).
따라서 지속 가능한 농업에서는 PGPR의 중요성이 대두되고 있으며, 특히 농업적으로 유익한 미생물을 작물에 대한 생물 비료 재료로 중요하게 사용할 수 있으므로, 인산 분해 미생물을 포함한 다양한 식물 생장 촉진 미생물들의 분리 및 특성을 규명하는 연구들이 널리 수행되고 있다 (Vessey, 2003; Bhattacharyya and Jha, 2012; Backer et al., 2018).
본 연구는 농업적으로 유익한 다양한 식물 생장 촉진 미생물을 분리하고자, 토양으로부터 서로 다른 8 종류의 Pseudomonas 종들을 분리하여, 분자생물학적인 동정을 수행함과 동시에 무기 인산 가용화 활성, 인돌 아세트산 및 지베렐린 생성 활성 및 ACC deaminase 활성 조사를 통하여 식물 생장 촉진 특성을 규명하고자 하였다.
Materials and Methods
미생물 균주 분리 및 분자생물학적 16S rDNA 동정
식물 생장 촉진 미생물을 분리하고자 순천시 서면 지본리 소재 순천대학교 부속 농장의 유기농 재배지 토양으로부터 시료를 채취하여 0.5% 인산칼슘 [Ca3(PO4)2]를 포함하는 Pikovskaya agar배지에 도말하여 인산 분해 활성을 보이는 균주를 분리하였다 (Pikovskaya, 1948). 분자생물학적 동정을 위하여 분리된 미생물을 이용하여 genomic DNA를 분리한 다음 16S rDNA 영역을 27F primer (5’-AGA GTTTGATCCCTGGCTCAG-3’)과 1492R primer (5’-GGTTACCTTGTTACGACTT-3’)을 이용하여 연쇄 증폭 반응 (polymerase chain reaction: PCR) 방법으로 확보하였다. 확보된 16S rDNA 연쇄 증폭 반응 산물을 Solgent 회사 (Daejeon, Korea)에 의뢰하여 염기서열분석을 수행한 후, BLAST analysis와 NCBI database (http://www.ncbi. nlm.nih.gov/BLAST)를 이용하여 유사 염기서열을 분석하였다. Phylogenic tree는 CLUSTAL X 프로그램을 이용하여 neighbor-joining 방법과 MEGA4 프로그램을 활용하여 분석하였다 (Saitou and Nei, 1987; Thompson et al., 1997; Kumar et al., 2001).
정량적 인산 분해 활성 및 pH 변화 측정
분리된 미생물들의 정략적인 인산 분해 활성을 측정하고자 0.5% Ca3(PO4)2가 함유 되어 있는 Pikovskaya 배양 배지에 미생물을 접종한 다음, 30°C 배양기에서 1일, 2일, 3일 및 5일간 단계적으로 배양한 후 원심 분리 방법으로 미생물 배양 상등액을 확보한 다음 molybdenum-blue 방법으로 인산 분해 활성을 조사하였고 (Murphy and Riley, 1962), pH 변화를 pH 미터기를 이용하여 측정하였다. 모든 실험은 3회 반복 수행하여 정량적인 분석으로 평균값으로 계산하였다.
인돌 아세트산 생성 활성 측정
인돌 아세트산 (IAA) 생성 활성은 Leveau와 Lindow 방법에 따라 측정하였다 (Leveau and Lindow, 2005). 분리된 미생물을 0.2% tryptophan이 함유되어 있는 King's medium에 24시간 배양한 다음, 배양액 상등액과 Salkowski's reagent를 1:2 (v/v)의 비율로 혼합 한 다음, Gordon과 Weber 방법 (Gordon and Weber, 1951)을 이용하여 발색 정도를 흡광 광도계 (UV-Visible Spectrophotometer, Shimadzu)를 이용하여 530 nm에서 흡광도를 측정하였다. 실험은 3 회 반복 수행 하였으며 정량적인 분석을 위하여 인돌 아세트산 (IAA) 표준 용액을 이용하여 표준 곡선을 활용하여 정량적인 분석을 수행하였다.
지베렐린 생성 활성 측정
지베렐린 호르몬 (GA3) 생성 활성 측정은 미생물 배양액 상등액 1 mL과 에탄올 1 mL 그리고 3.75 M 염화수소 (HCl) 8 mL을 첨가하여 10 mL 되게 한 후 10초간 혼합하여 실온에서 5분 정도 둔 다음 흡광 광도계로 254 nm 흡광도를 측정하여 정량적으로 분석하였다 (Holbrook et al., 1961). 실험은 3 회 반복 수행 하였으며 정량적인 분석을 위하여 지베렐린 (GA3) 표준 용액을 이용하여 표준 곡선을 활용하여 정량적인 분석을 수행하였다.
ACC deaminase 활성 분석
ACC deaminase 활성의 양을 측정하기 위해, ACC분해되고 난 후 생성되는 α- ketobutyrat를 분석하였다. ACC deaminase 활성은 시간당 단백질 mg 당 생산된 α-ketobutyrate양으로 표현되었다 (Penrose and Glick, 2003). 실험은 3 회 반복 수행 하였으며 정량적인 분석을 위하여 α-ketobutyrate표준용액을 이용하여 표준 곡선을 활용하여 정량적인 분석을 수행하였다.
상추 생장 촉진 활성 조사
분리된 미생물의 식물 생육 촉진 능력을 측정 하기 위하여, 상추 생육 비교 실험을 수행하였다. 분리된 미생물을 LB배지에 30°C, 200 rpm 조건의 배양기에서 overnight 배양 한 후, 6일간 생육 시킨 상추가 존재하는 pot 당 균주 수를 108 cfu mL-1 농도에 맞춰 각각 100 mL을 접종 한 다음, 2주 후에 생체량 및 상층부 생장 길이를 측정하여 비교하였다. 모든 실험은 3반복 이상 수행하여 평균값을 측정하였다.
통계분석
모든 실험 data는 SAS package (SAS, 1999) 를 이용한 ANOVA (analysis of variance)에 적용하여 분석하였다. 다양한 처리 방법들 사이의 차이는 5% (p ≤ 0.05) 확률 유의 수준에 해당하는 LSD (least significant differences test)를 사용하여 비교하였다 (Steel and Torrie, 1980).
Results and Discussion
인산 분해 미생물 Pseudomonas species 분리 및 16S rDNA 분자생물학적 동정
무기 인산염 분해 능력을 가진 미생물을 분리하고자 순천시 서면 지본리 소재 순천대학교 부속 농장의 재배지 토양시료를 채취한 다음 0.5% Ca3(PO4)2가 포함된 Pikovskaya agar 배지에 도말한 다음 3일 후 투명 환 (clear zone)을 보이는 약 50여종의 미생물을 확보하였다. 16S rDNA 염기서열 분석방법으로 분리된 미생물들을 확인한 결과, 그중 8 종의 Pseudomonas species를 확보하였으며 이들을 각각 PM1 - PM8으로 명명한 다음 16S rDNA 염기서열을 이용하여 BLAST search 와 phylogenic tree 방법으로 분석한 결과, PM1은 Pseudomonas chlorophis, PM2는 Pseudomonas cedrina, PM3은 Pseudomonas fragi, PM4는 Pseudomonas corrugata, PM5는 Pseudomonas putida, PM6은 Pseudomonas jessenii, PM7은 Pseudomonas koreensis, PM8은 Pseudomonas tolaasii 로 확인되었다 (Fig. 1). 이들 모든 종들은 대표적인 식물생장촉진 미생물로 알려진 Pseudomonas fluorescens 및 Pseudomonas putida 그룹에 포함되는 것으로 확인되었다 (Garrido-Sanz et al., 2016).
일반적으로 Pseudomonas 미생물은 다양한 환경에 널리 분포하고 있으며 현재까지 100종이 넘는 종이 알려지고 있다. 특히 Pseudomonas fluorescens 그룹으로 분류되어지고 있는 몇몇 종들 (Pseudomonas brassicacearum, Pseudomonas protegens, Pseudomonas chlororaphis 및 Pseudomonas fluorescens 등)은 식물 생장 촉진 호르몬 및 대사 물질 생성, 항생제 생산 및 식물의 전신 저항 반응 유도에 의한 식물 병 억제 능력을 가짐으로써 식물 생장 촉진 미생물로 보고 되어지고 있다 (Ellis et al., 2000; Loper et al., 2012; Garrido-Sanz et al., 2016).
따라서 본 연구에서 분리된 서로 다른 8 종류의 Pseudomonas 미생물들의 식물 생장 촉진 활성에 대한 특성을 비교 분석하고자 하였다.
인산 분해 활성 능력 측정
분리 확보된 8 종류의 Pseudomonas species (PM1 - PM8)들의 무기 인산염 분해 활성을 확인한 결과 (Fig. 2), 모든 균주들은 Pikovskaya 고체 배지에서 매우 높은 무기 인산 분해 활성을 보였고 그 중에 PM7 균주가 가장 높은 활성을 나타내었다 (Fig. 2A). 정량적인 무기 인산 분해 능력을 분석한 결과, 대부분의 Pseudomonas 미생물 종들 (PM1 - PM4, PM6, PM8)의 경우 접종 후 2일차에 가장 높은 활성을 보인 후 점차적으로 감소하는 경향을 보였다. PM5의 경우는 접종 1일차에 가장 높은 활성을 보인 후 점차 감소하는 경향을 보인 반면, PM7의 경우 1일부 5일까지 큰 변화없이 오랫동안 지속적으로 높은 활성을 보였다 (Fig. 2B). 같은 조건에서의 pH 변화를 0일, 1일, 2일, 3일, 5일 배양한 후 상등액을 측정한 결과에 의하면, 대부분의 미생물들 (PM1 - 6, PM8)의 인산 분해 활성은 pH가 가장 낮은 2일차에 가장 높은 활성을 보이다가 pH가 점차 증가함에 따라 분해 활성이 낮아지는 결과를 보였고, PM7의 경우 5일째까지 약 pH 4정도로 나타남에 따라 인산분해활성은 pH 감소와 상당한 연관성이 있는 것으로 나타났다 (Fig. 2C).
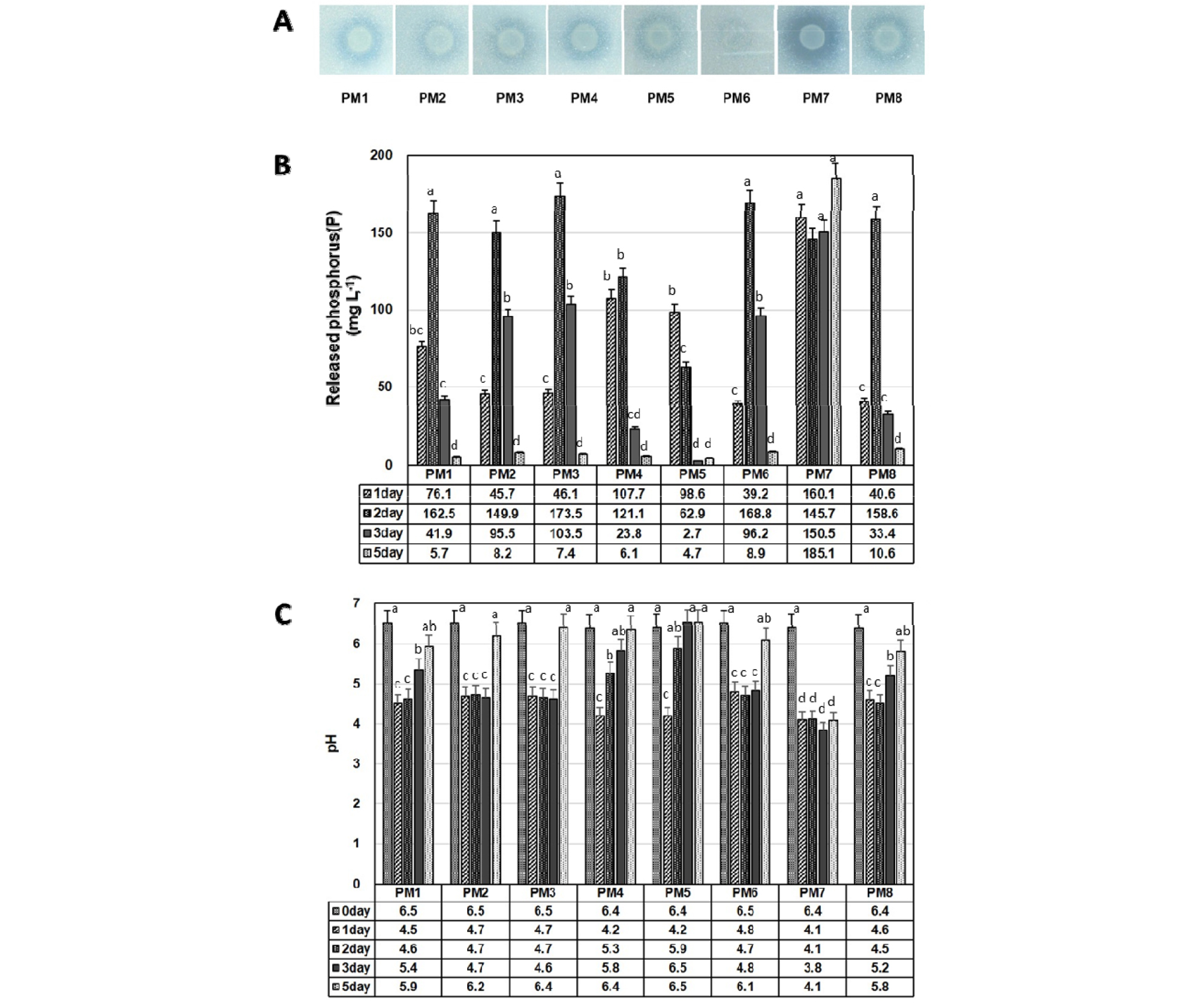
Fig. 2.
Plate assay (A) and liquid assay (B) for phosphate solubilizing activity and pH change (C) of 8 Pseudomonas species (PM1 - PM8). The numbers above the bars mean the average number each condition, respectively, from 3 replicate experiments. Means within each error bars and letters are significantly different the SD by LSD at p ≤ 0.05, respectively.
일반적으로 미생물에 의한 무기 인산 분해 활성은 미생물이 생성하는 글루코니산 (gluconic acid)등 다양한 유기산에 의해 중요하게 영향을 받는 것으로 알려져 있으며, 많은 인산 분해 미생물의 경우 인산 분해 활성은 pH 감소와 상관성을 보여주었다 (Castagno et al., 2011; Sharma et al., 2013). 따라서 본 연구에서 분리된 8 종류의 미생물들 역시 다양한 유기산 생성으로 pH를 감소시키면서 무기 인산 분해 활성을 보이는 것으로 생각된다.
일반적으로 미생물 생태와 높은 유기물을 가진 토양은 기존의 관리 토양보다 비료 요구량이 더 낮은 것으로 알려져 있다 (Bender et al., 2016). 따라서, 토양에서의 유기 영양 공급원이 적용 될 때 식물 뿌리에 의해 접근되는 표면적 확대, 질소 고정, 인산 가용화, 측근 포자 생성 및 HCN 생산 등의 기능을 가지는 식물 생장 촉진 미생물 (PGPR)활동이 종종 중요하게 고려된다 (Beattie, 2015; Pii et al., 2015). 특히 많은 식물 영양소 중 가장 제한적인 영양소는 인산으로 알려져 있다. 인산의 경우 대부분의 농업용 토양에는 충분한 양이 포함되어 있지만 대부분 비수용성 형태로 존재하며, 불용성 인산염을 가용화 형태로 만드는 인산 가용화 미생물의 경우 일반적으로 식물 생장 촉진 미생물의 중요한 하나의 종류로 알려지고 있다. 따라서 분리된 8종류 Pseudomonas 미생물의 경우 높은 인산 분해 능력 활성을 가지므로 식물 생장 촉진 미생물로서의 역할을 할 수 있으리라 생각된다.
인돌 아세트산 및 지베렐린 식물호르몬 생성 활성 측정
많은 인산 분해 활성을 가지는 미생물의 경우 일반적으로 식물 생장을 촉진하는 것으로 알려져 있으며, 특히 중요한 식물 호르몬 중의 하나인 인돌 아세트산 (IAA)과 지베렐린 (GA) 생성으로 식물 생장을 촉진하는 기작이 대표적으로 알려져 있다 (Omer et al., 2004; Gupta et al., 2015). 따라서 분리된 인산 분해 미생물 (PM1 - 8) 들의 인돌 아세트산과 지베렐린 생성 활성을 측정하였다 (Fig. 3). 인돌 아세트산 호르몬 생성 활성 경우 PM1, PM4, PM5, PM7의 네 종류 미생물이 높은 생성 활성을 보였고 나머지 미생물의 경우에는 활성을 보이지 않았다. 특히 이들 중 PM7 종이 가장 높은 활성을 보였다 (Fig. 3A). 지베렐린 생성의 경우, PM4, PM5, PM7, PM8의 네 종류 미생물이 높은 생성 활성을 보였고 나머지 미생물의 경우에는 활성을 보이지 않았다. 특히 PM5과 PM7 미생물이 가장 높은 활성을 보였다 (Fig. 3B). 최종적으로 PM4, PM5, PM7 미생물의 경우 IAA 및 GA 생성능력을 모두 가지는 것으로 확인되었다. 대부분의 식물 생장 촉진 미생물의 경우 인산 분해 능력뿐만 아니라 인돌 아세트산과 지베렐린등 식물 생장 촉진 호르몬 생성하여 궁극적으로 식물 생장을 촉진하는 기능을 가지는 것으로 알려져 있다 (Leveau and Lindow, 2005; Lugtenberg and Kamilova, 2009; Bhattacharyya and Jha, 2012). 따라서 본 연구에서 분리된 일부 Pseudomonas 미생물인 경우, 인산 분해 능력뿐만 아니라 인돌 아세트산과 지베렐린 같은 식물생장호르몬을 생성함으로써 잠재적으로 식물생장촉진 활성을 가지는 것으로 생각된다.
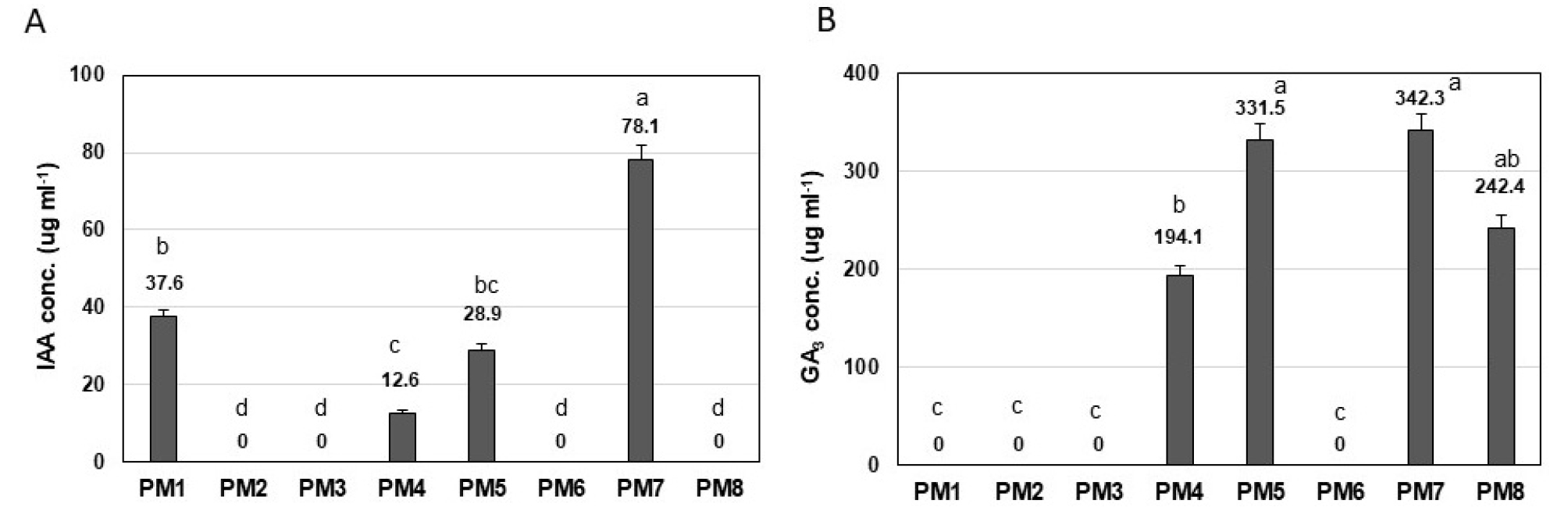
Fig. 3.
Production of plant hormone IAA (A) and GA3 (B) from 8 Pseudomonas species (PM1 - PM8). The numbers below the bars mean the average number each condition, respectively, from 3 replicate experiments. Means within each error bars and letters are significantly different the SD by LSD at p ≤ 0.05, respectively.
ACC deaminase 활성의 정량적 측정
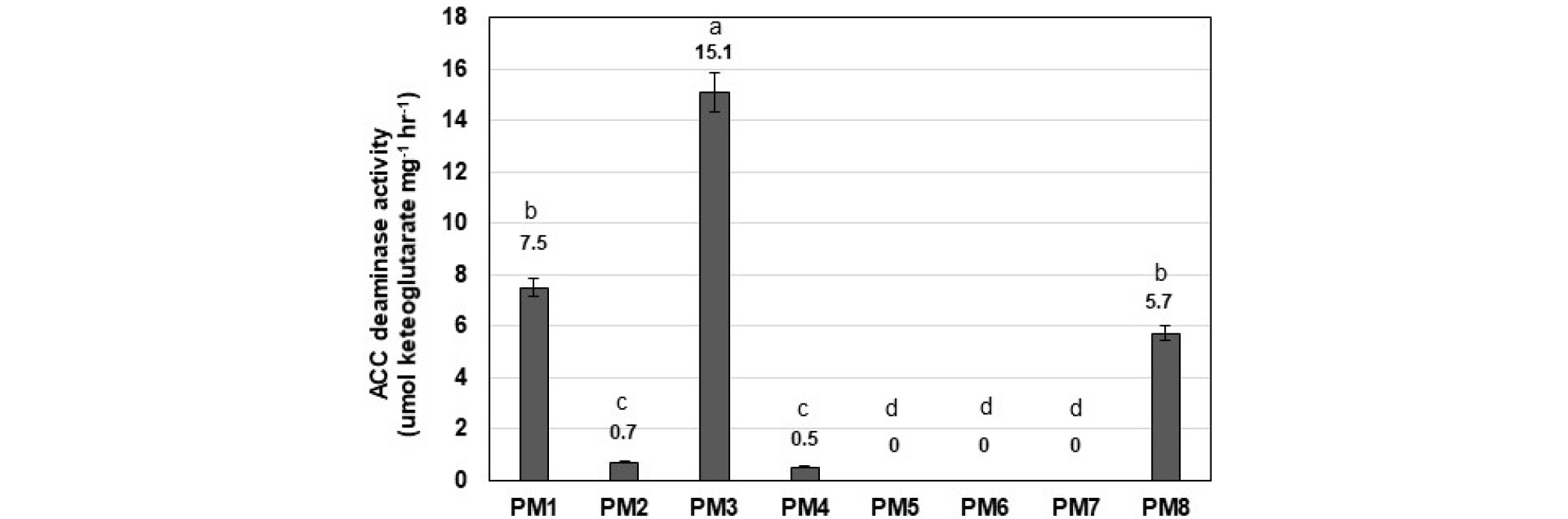
일반적으로 에틸렌은 매우 낮은 농도에서 활성을 가지는 기체 성분 호르몬이며, 다양한 스트레스 동안 높은 농도 증가를 보이는 “스트레스 호르몬”으로 식물의 생장을 저해하는 것으로 알려져 있다 (Morgan and Drew, 1997). 따라서 전구체인 1-aminocyclopropane-1-carboxylic acid (ACC)를 분해시키는 ACC deaminase활성을 가지는 PGPR 미생물의 경우 식물에서 에틸렌 생산을 감소시켜 식물의 스트레스 내성 증진 및 식물 생장 촉진을 하는 것으로 알려지고 있다 (Glick, 2014; Heydarian et al., 2016; Gupta and Pandey, 2019).
분리된 Pseudomonas 미생물들 중에서 PM1, PM3, PM8의 경우에는 높은 활성을 보였고 PM2 및 PM4의 경우에는 매우 낮은 활성을 보였다 (Fig. 4).
식물 생장 촉진 활성
분리된 8 종류의 Pseudomonase 균주들은 인산 분해 활성, 식물호르몬 인돌 아세트산과 지베렐린 생성 능력, ACC deaminase활성등을 가지고 있으므로, 식물 생장 촉진 활성을 검정하고자 어린 상추 식물을 대상으로 균주 접종 후 생체량 및 상층부 길이 생장등 식물의 생장 특성을 조사하였다 (Fig. 5).
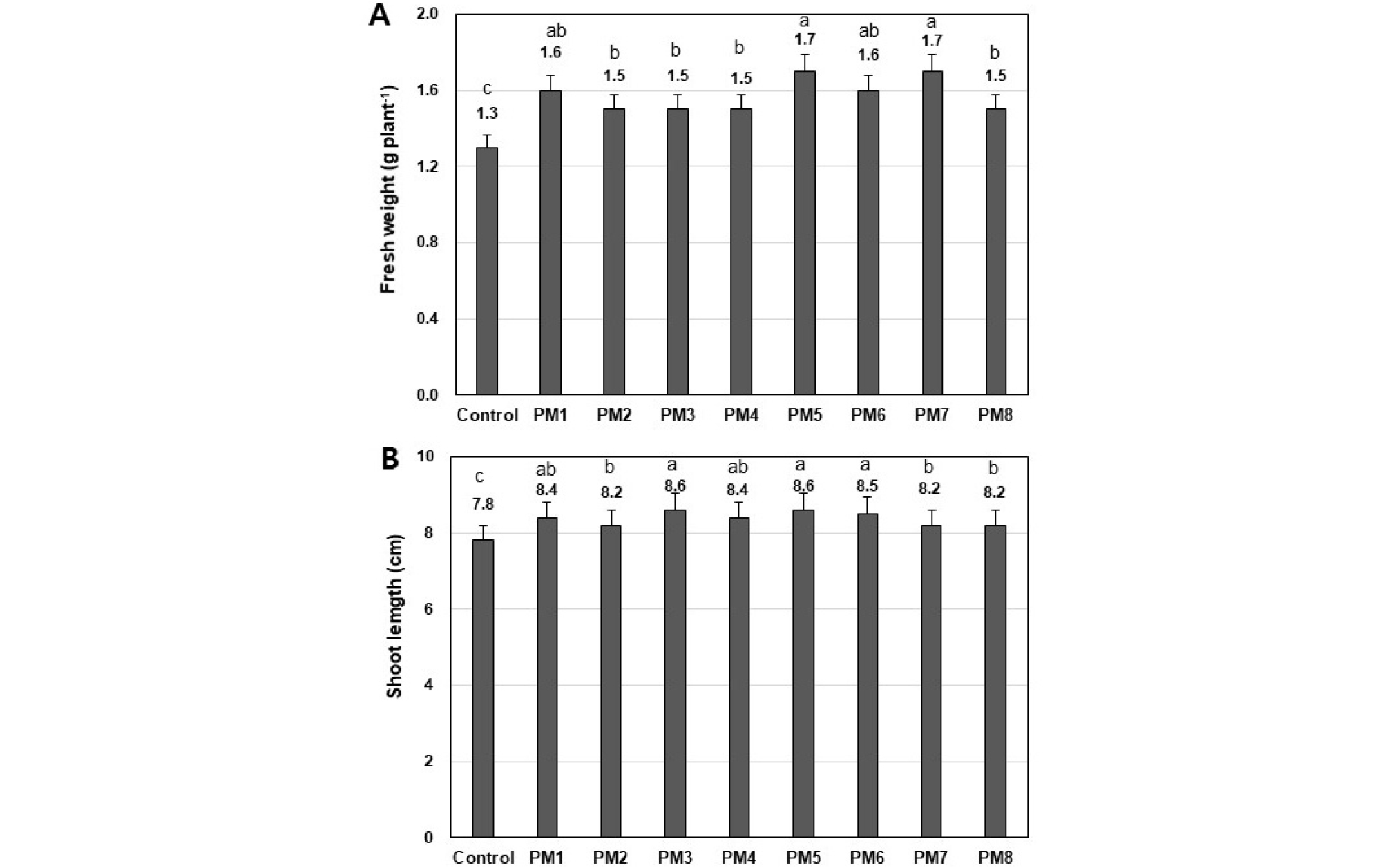
Fig. 5.
Effects of isolated 8 Pseudomonas species (PM1 - PM8) inoculation on growth of lettuce seedlings. The numbers mean the average number on fresh weight (g plant-1) (A) and shoot length (cm plant-1) (B) from 10 independent plants each condition, respectively. Means within each error bars and letters are significantly different the SD by LSD at p ≤ 0.05, respectively. All data was analyzed from 3 replicate experiments.
처리된 8 종류의 미생물 경우 모두 식물의 생장을 촉진시키는 활성으로 보였으며 생체량 (fresh weight)의 경우 대조구의 경우 1.3 ± 0.08 g plant-1를 보인 반면, 미생물 처리구의 경우 1.5 - 1.7 ± 0.1 g plant-1를 보여 대조구에 비해 15 - 30%의 증진효과를 보였다. 상층부 길이 생장 (shoot length)의 경우에도 대조구에 비해 5 - 10% 증가를 보였다. 특이 PM5과 PM7의 경우 다른 분리된 미생물들 보다 가장 높은 생체량 증진 효과를 보였다. Fig. 3의 결과에서 보는 와 같이, PM5과 PM7 미생물의 경우 둘다 높은 IAA 및 지베렐린 생성 활성을 보여 이들과의 연관성이 있는 것으로 생각된다. PM6 미생물의 경우 IAA 및 GA생성능력, ACC deaminase 활성 능력을 보이지는 않았지만 Fig. 2에서 보이는 것처럼 매우 높은 인산 분해 활성을 가지고 있으므로 식물의 영양소 가용화 및 흡수 효율을 높이는 기작으로 식물 생장을 촉진시키는 활성을 가지고 있는 것으로 생각된다.
보고된 많은 식물 생장 촉진 미생물들 역시 인돌 아세트산 혹은 지베렐린 등의 식물 생장 호르몬 생성 및 무기 인산염등 영양소의 가용화 작용으로 식물 생장을 촉진하는 것으로 알려져 있다 (Vessey, 2003; Santoro et al., 2015).
따라서 전 세계적으로 지속 가능한 친환경 유기 농업의 관심 증대로 인하여 생물 비료와 생물 농약의 중요성이 대두되고 있으며 많은 연구자들에 의해 다양한 유용미생물들이 보고 되고 있다. 본 연구에서 분리된 8 종류의 미생물들 역시 친환경 농업에 적용될 수 있는 인산 분해 활성, 식물 생장 호르몬 생성 등 다양한 생물비료특성 및 식물 생장 촉진 특성을 보이므로 이들 미생물을 미생물비료 재료로 이용하여 경작지에 적용한다면 농가의 수익증대에 기여할 수 있을 것으로 생각된다.