Introduction
Materials and Methods
공시토양
시험포장 및 재배관리
암모니아 가스 시료채취 및 분석
토양 이화학적 특성 및 배추 수량 조사
통계분석
Results and Discussion
암모니아 휘산
토양특성 변화
배추 수량
Conclusions
Conclusions
Introduction
2016년 국내 NH3 총 배출량은 301,301 톤으로 추정되고 있으며, 농업부문에서 237,017 톤 (78.7%)으로 가장 많이 배출되고 있다 (NIER, 2019). 특히 토양에 요소, 질산암모늄 등과 같은 질소질 비료를 시비할 때 다량의 NH3가 휘산된다. 토양 내 암모늄 이온 (NH4+)은 아래 식과 같이 수산화 이온 (OH‒)과 반응하여 기체상태인 NH3로 전환되고 다량의 NH3가 대기 중으로 휘산된다.
(Du Plessis and Kroontje, 1964)
암모니아 휘산은 질소 손실이라는 경제적 손실뿐만 아니라 자연환경에 미치는 부정적인 영향도 가지고있다. 일반적으로 대기 중 암모니아 (NH3) 농도는 1 - 20 ppb로 매우 낮지만 대기화학, 자연생태계의 산성화, 생물상의 다양성 변화에 크게 영향을 미치는 것으로 알려져 있다 (Gundersen and Rasmussen, 1990; Bobbink et al., 1992; Asman, 1994).
특히, 암모니아 (NH3)는 대기 중에서 황산화물이나 질소산화물 등과 반응하여 황산암모늄 (NH4SO4)이나 질산암모늄 (NH4NO3) 등의 형태인 2차 미세먼지 (PM2.5, Secondary particulate matter)를 생성하며 미세먼지의 전구물질로서 작용한다 (Anderson, 2003). PM2.5는 지름이 2.5 µm 이하의 미세한 입자를 뜻하며 일반 먼지와는 다르게 코와 기관지에서 걸러지지 않고 체내 축적되어 호흡을 통해 기관지, 폐에 직접적으로 영향을 끼친다 (Pope and Dockery, 2006). 또한 호흡 과정에서 혈액으로 들어가 뇌졸중, 심장마비 등의 여러 문제를 야기하고 당뇨병 등 다른 질환에도 영향을 끼친다.
일반적으로 NH3는 토양 내 pH가 높아지면 OH‒가 NH4+과 반응하며 NH3의 형태로의 전환이 빠르게 이루어진다 (Kim et al., 2020; Lee et al., 2020). 특히, 토양의 pH가 7.0 이상일 때 NH4+이 NH3로 전환되어 대기 중으로 손실될 수 있는 적정 조건이라고 알려져 있다 (Hillel and Hatfield, 2005). 따라서 토양의 pH를 낮춤으로써 NH3의 휘산량을 저감시킬 수 있다.
토양의 pH를 낮추기 위해 황산철 (FeSO4)과 황산알루미늄 [Al2(SO4)3] 등을 이용할 수 있다. 그러나, Al2(SO4)3은 알루미늄을 포함하고 있어 농경지 토양에 과량으로 시용 시 알루미늄 독성에 의한 작물의 생육 저하를 야기할 수 있다. FeSO4는 토양의 pH를 저감시킬 뿐만 아니라 작물의 다량 필수원소인 황 (S)과 미량 필수원소인 철 (Fe)을 동시에 함유하고 있어 작물의 생육에 이로울 수 있다. 다만 Fe은 미량 필수원소인 반면에 작물이 과량으로 흡수 시 독성을 야기할 수 있어 농경지 토양에서는 적정량으로 시용하여야 한다. 이전 연구에 따르면, 계사에서 사용되는 짚에 FeSO4・7H2O를 100과 200 g kg-1의 수준으로 처리했을 때 짚의 pH를 감소시킴으로써 발생된 누적 암모니아가 각각 11과 58%만큼 감소하였다고 보고하였다 (Moore, 1995). 하지만 FeSO4를 농경지 토양에 처리했을 때 발생하는 암모니아의 저감 효과 및 작물의 수량에 미치는 영향에 대한 연구는 미비한 실정이다. 따라서 본 연구는 토양의 pH를 저감시킬 수 있는 제재인 FeSO4가 PM2.5의 원인 물질인 NH3의 휘산 및 작물의 생산성에 미치는 영향을 조사하여 적정 시용량을 산정하기 위해 실시되었다.
Materials and Methods
공시토양
본 연구를 수행하기 위해 경남 밀양시 부북면 오례리에 소재하는 부산대학교 부속농장 (35°30'08.1"N, 128°43'18.2"E)의 밭토양을 공시토양으로 선정하였다. 시험포장의 토양은 용지통 (Fine loamy, mixed, mesic family of Typic Paleudults with 7 - 15% slope, moderately well drained)으로 모래, 미사, 점토의 함량이 각각 42.5%, 44.7%, 12.8%로 토성은 양토였다. 시험 토양의 pH는 7.2이었으며 총 질소 함량과 암모늄태 질소의 함량은 각각 0.90 g kg-1과 6.15 mg kg-1이었다. 자세한 공시토양의 화학적 특성은 Table 1에 나타냈다.
Table 1.
Selected chemical properties of the studied soil before the test (n = 3).
시험포장 및 재배관리
밭토양에서 제재 처리에 따른 NH3 휘산량과 토양 특성 및 작물수량에 미치는 영향을 조사하기 위하여 2020년 4월 8일에 배추 (Brassica rapa L.) 모종을 65 cm × 40 cm 간격으로 정식하여 6월 10일에 수확하였다.
FeSO4 시용에 따른 NH3 휘산량 저감 효과를 조사하기 위하여 FeSO4・7H2O를 0, 50, 100, 200 kg Fe ha-1로 시용하였다. 모든 처리구에 N-P2O5-K2O (113-78-79 kg ha-1)를 기비로 4월 7일에 시비하였으며 추비로 4월 21일, 5월 6일, 5월 20일에 각각 60-0-26, 73-0-66, 73-0-26 kg ha-1를 시비하였다. 각 처리구의 크기는 2.3 × 2.4 m (5.52 m2)이었으며 난괴법 (Randomized complete block design)에 따라 3반복하여 배치하였다.
암모니아 가스 시료채취 및 분석
밭토양에서 발생하는 NH3 가스를 측정하기 위해서 static chamber 법 (Nômmik, 1973)을 모방하여 실험에 적용시켰다. 면적이 0.01 m2인 챔버를 각 처리구의 두둑 정 중앙에 5 cm 깊이로 설치하였고 주 5회 NH3 가스 시료를 채취하였고 수확 후에는 주 1회 가스 시료를 채취하였다. 재배기간 동안에는 챔버 안에 식물체가 자라지 않게 하였다. 챔버 내에는 2 cm 두께의 스펀지 2개가 설치되어 있다. 위쪽에 위치한 스펀지는 대기 중에 존재하는 NH3 가스가 챔버 내부로 들어오지 못하게 막는 것이고 아래쪽에 위치한 스펀지가 토양으로부터 발생하는 NH3 가스를 포집하는 역할을 한다. 두 개의 스펀지 모두 60 ml의 glycerol (4%) + H3PO4 (1M) 혼합용액으로 충분히 적신 후 비닐백에 보관하여 사용하였다. 가스 시료채취 시 사용된 스펀지는 모두 새 것으로 교체하였고 아래쪽 스펀지는 150 ml의 2 M KCl용액이 담긴 플라스틱 밀폐 용기에 완전히 담근 후 실험실로 옮겨졌다. 침출용액 중에 존재하는 NH4+은 Indophenol blue 비색법 (Searle, 1984)을 통해 UV/VIS Spectrophotometer를 이용하여 667 nm의 파장에서 측정하였고 이를 이용하여 NH3-N의 휘산량을 계산하였다.
토양 이화학적 특성 및 배추 수량 조사
토성은 비중계법으로 분석하여 미국농무성법 분류기준으로 분류하였다. 제재 투입에 따른 토양 화학성 변화를 알아보기 위해 시험 전 토양과 배추 수확 후 토양을 Auger를 이용하여 채취한 후 분석에 이용하였다. pH 및 전기전도도 (Electrical conductivity, EC)는 1:5 (토양 : 물) 비율로 30분간 교반하여 pH meter (Orion Star A215, Thermo Fisher Scientific, USA)로 측정하였다. 총 질소 함량은 Kjeldahl법을, 유기물 함량은 Wakley and Black법 (Nelson and Sommers, 1996)을 이용하여 분석하였다. 유효인산 함량은 Lancaster method (RDA, 1988)을 이용하여 UV-VIS Spectrophotometer로 흡광도를 측정하여 분석하였다. 치환성 양이온은 1 M NH4OAc (pH 7.0)로 침출하여 atomic absorption spectrometer (AA-7000, Shimadzu, Japan)로 측정하였다. 토양 내 무기태 질소의 함량은 토양 건조시료 5 g과 25 ml의 2 M KCl 용액을 30분 동안 진탕한 후 Whatman No. 2로 여과하여 침출액을 실험에 이용하였다. 암모늄태 질소 (NH4+-N)는 UV-VIS Spectrophotometer로 667 nm의 파장에서 농도를 측정하는 indophenol blue 비색법 (Searle, 1984)으로 분석하였고 질산태 질소 (NO3‒-N)는 brucine 법 (Wolf, 1944)으로 분석하였다.
수확한 배추는 드라이 오븐을 이용하여 70°C에서 72시간 이상 건조시킨 후 건물중을 측정하였다.
통계분석
수확 후 토양의 NH3 누적 배출량, pH, NH4+ 함량의 통계 분석을 위해 Statistix 통계 프로그램 (version 9.0, Analytical Software, Tallahassee, USA)을 이용하였다. 처리구간 차이를 비교하기 위하여 조사된 자료는 ANOVA 검증을 통하여 분석하였다. F-test 결과 값이 p < 0.05의 범위에서 유의한 경우에만 최소유의차 검정 (Least significant difference)을 실시하였다.
Results and Discussion
암모니아 휘산
배추의 재배기간 동안 NH3의 일일 배출량의 경향은 전반기에 대부분의 NH3가 발생하였으며 후반기에는 발생량이 적게 나타났다 (Fig. 1a). NH3의 일일 배출량 변화와 대기 및 토양온도와의 관계를 파악하기 위해 배추의 재배기간 동안 일일 대기 및 토양온도를 조사하였으나 NH3의 일일 배출량과 대기 및 토양온도와의 밀접한 관계는 나타나지 않았다. 일반적으로 토양의 온도가 증가할수록 NH3의 발생량이 증가한다. He (1999)은 토양의 온도가 5°C에서 25°C, 25°C에서 45°C로 증가할 때 NH3 최대 배출량이 각각 2배, 3.4배 증가한다고 보고하였다. 배추를 정식한 4월 8일부터 5월 2일까지 일일 평균 대기 및 토양온도는 각각 17.2°C와 18.5°C로 상대적으로 낮게 유지되었으나 5월 3일 이후 대기 및 토양온도는 점차 증가하는 경향을 나타냈다 (Fig. 1b). 그러나 배추재배 기간 동안 일일 NH3의 배출량은 상대적으로 온도가 낮게 유지되었던 4월에 상대적으로 높게 나타났다.
배추의 재배기간 동안 일일 NH3의 배출량 변화와 토양수분과의 관계를 파악하기 위해 일일 강수량 및 토양 공극 내 수분이 차지하는 비율 (water filled pore space, WFPS)를 조사하였다 (Fig. 1c). 배추 재배기간 동안 일일 NH3 배출량의 피크는 4월 16일, 4월 27일, 5월 12일, 5월 24일 총 4회에 걸쳐 나타났다. 일일 강수량 및 WFPS가 상대적으로 높았던 시기는 4월 17일, 5월 7일, 6월 14일로 조사되어 일일 NH3 배출량의 급격한 증가와 토양수분함량과는 큰 관련성이 없는 것으로 나타났다. WFPS가 47% 정도에서는 요소의 분해가 빠르게 일어나면서 NH3의 휘산이 잘 일어나지만, WFPS가 59% 이상인 조건에서 토양의 대공극 내 수분의 함량이 많아지면서 오히려 NH3의 휘산이 방해된다 (Pelster, 2019). 그러나 본 연구에서 일일 NH3의 배출량이 상대적으로 높게 나타났던 4월 16일부터 4월 29일 사이의 평균WFPS는 60%로 높게 나타났다. 따라서 본 연구에서 배추 재배 기간 동안 일일 NH3 배출량 변화는 온도와 토양수분과 같은 기후인자 보다는 배추 재배기간 동안 시용된 요소비료에 영향을 받은 것으로 판단된다. 요소비료는 기비로 4월 7일, 추비로 4월 21일, 5월 6일, 5월 20일에 시용되었으며 일일 NH3 배출량의 피크는 질소비료가 시용된 후 몇일 뒤 4월 16일, 4월 26일, 5월 12일, 5월 24일에 발생했다 (Fig. 1a). 일반적으로 농경지 토양에 요소비료가 시용된 후 약7일 후에 NH3가 급격하게 발생한다 (Jantalia, 2012). 본 연구에서 기비와 추비 시 다소 차이는 있었지만 요소비료 시용 후 4~9일 사이에 NH3가 급격하게 발생한것으로 조사되었다. 요소비료는 기비로 4월 7일 113 kg N ha-1로 시용되었으며, 추비로 4월 21일, 5월 6일, 5월 20일에 60, 73, 73 kg N ha-1로 각각 시용되었다. 따라서 상대적으로 많은 양의 요소가 시용된 4월 7일과 4월 16일 이후에 일일 NH3의 배출량이 급격하게 증가한 것으로 조사되었다.
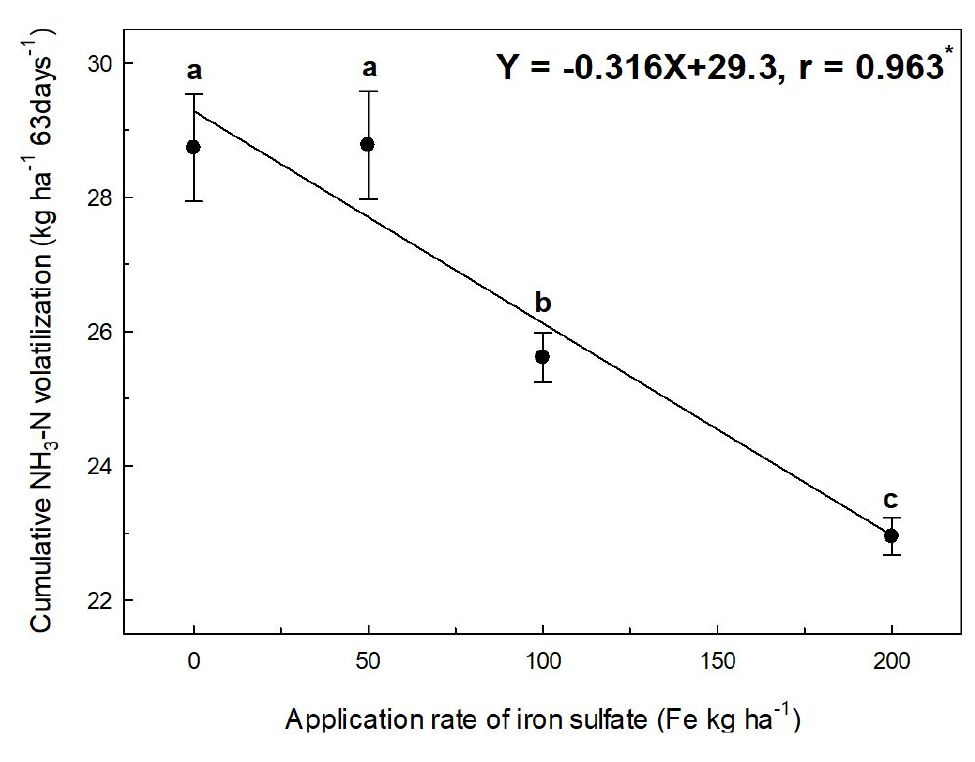
배추 재배기간 총 63일간 누적 NH3 배출량은 FeSO4의 시용량을 증가시킴에 따라 유의하게 감소하는 경향을 나타냈다 (Fig. 2). FeSO4를 50 kg ha-1로 시용하였을 때 NH3의 누적배출량은 무처리에 비해 유의하게 감소되지 않았으나 시용량을 100과 200 kg ha-1로 증가시켰을 때 유의하게 감소하였다. 또한 FeSO4를 200 kg ha-1로 시용하였을 때 무처리에 비해 NH3의 누적배출량을 약 21%까지 저감 시키는 효과를 나타냈다. Moore (1996)은 돈분 슬러리에 FeSO4를13 g kg-1과 26 g kg-1을 투입하였을 때 무처리에 비해 NH3 배출량을 각각 53%와 77% 감소시켰다고 보고하였다.
토양특성 변화
배추 수확 후 토양의 pH는 FeSO4의 시용량을 증가시킴에 따라 감소하는 결과를 나타냈다 (Table 2). 토양에 FeSO4를 시용하게 되면 아래의 반응식에 의해 Fe2+가 Fe3+로 산화되면서 최종적으로 2몰의 H+를 생성하여 토양의 pH는 낮아지게 된다 (Xenidis, 2010).
Table 2.
Change of pH of soils amended with different rates of FeSO4 after harvest time.
| Application rate (kg Fe ha-1) | pH (1:5, H2O) | SD |
| 0 | 7.26a | 0.01 |
| 50 | 7.12a | 0.06 |
| 100 | 6.97ab | 0.07 |
| 200 | 6.57b | 0.11 |
Warren and Alloway (2003)의 연구결과에 따르면 토양에 FeSO4・7H2O를 0, 0.22, 0.54, 1.09% (w w-1) 수준으로 처리하였을 때 토양의 pH가 6.9에서 각각 5.28, 3.96, 3.17로 감소하였다. 본 연구에서 FeSO4를 200 kg ha-1까지 시용하였을 때 토양의 pH는 7.26에서 6.57로 약 0.69 정도 감소되는 효과를 나타냈다. Warren and Alloway의 연구에서 보다 토양의 pH 감소효과가 낮았던 이유는 본 연구에서 FeSO4 200 kg ha-1을 중량비로 환산하면 약 0.01% (w w-1)로 Warren and Alloway의 연구에서 처리된 양 보다 낮았기 때문으로 판단된다.
토양의 pH가 낮아지게 되면 아래의 반응식과 같이 NH4+이 OH‒과 반응하여 기체상태인 NH3로 전환되어지는 과정이 저해되어 NH3의 누적배출량이 저감하게 된다.
(Du Plessis and Kroontje, 1964)
이러한 주장은 FeSO4 시용량에 따른 배추 수확 후 토양 내 NH4+함량 변화에 의해 입증된다. 배추 수확 후 토양 내 NH4+함량은 FeSO4의 시용량을 증가시킴에 따라 증가하는 결과를 보였다 (Table 3).
Table 3.
Change of NH4+ in soils amended with different rates of FeSO4 after harvest time.
| Application rate (kg Fe ha-1) | NH4+ (mg kg-1) | SD |
| 0 | 4.21b | 0.30 |
| 50 | 4.58b | 0.53 |
| 100 | 5.29ab | 0.24 |
| 200 | 6.23a | 0.22 |
배추 재배 기간 동안 누적 NH3 배출량은 수확 후 토양의 pH 변화와 유의한 정의 상관관계 (r = 0.676*)를 나타냈다 (Fig. 3a). 또한 배추 수확 후 토양의 pH 변화와 토양 내 NH4+함량은 유의한 부의 상관관계 (r = 0.663*)를 나타냈다 (Fig. 3b). 즉, 이상의 결과들을 바탕으로 볼 때 FeSO4의 시용량을 증가시킴에 따라 토양의 pH는 감소하였으며 토양의 pH가 감소함에 따라 NH4+가 NH3로 전환되는 과정이 저해되었으며 토양 내 NH4+의 함량은 증가하였다. 이러한 반응의 결과로 인하여 FeSO4의 시용량을 증가시킴에 따라 배추 재배 기간동안 NH3의 누적배출량은 감소하는 결과를 나타냈다.
배추 수량
FeSO4의 시용량에 따른 수확 후 배추의 건물수량은 Fig. 4에 나타냈다. 배추의 수량은 FeSO4 시용량 간에 통계적으로 유의한 차이는 없었으나 FeSO4의 시용량을 100 kg ha-1까지 증가시킴에 따라 증가하는 경향을 보이다가 200 kg ha-1로 시용량을 증가시켰을 때 다소 감소하는 경향을 나타냈다. 유사한 연구결과가 Fu (2013)에 의해 보고되었으며 해당 연구결과에 따르면 FeSO4를 0, 3, 6, 9, 12 g kg-1의 수준으로 처리했을 때 차나무의 건물수량이 무처리구에 비해 증가하다가 감소하는 경향을 나타내었다. 수량 반응식을 이용하여 배추의 수량은 FeSO4의 시용량 (FS)과 다음과 같은 관계가 있었다.
수량반응식을 이용하여 배추의 최고수량을 산정하여 본 결과, FeSO4를 110 kg ha-1로 시용 시 배추의 수량은 7.10 Mg ha-1로 나타났다. Fig. 2에서 나타난 바와 같이 배추 재배기간 동안 누적 NH3배출량은 FeSO4의 시용량 (FS)과 다음과 같은 관계가 있었다.
위의 관계식을 이용하여 배추의 최고수량을 얻었던 FeSO4의 시용량인 110 kg ha-1로 시용 시 NH3 누적 배출량은 25.8 kg ha-1 63 days-1으로 무처리에 비해 10.2% 저감되는 효과를 나타냈다. 따라서 FeSO4를 적정량으로 시용하면 PM2.5의 원인물질인 NH3의 발생량을 저감하면서 작물의 생산성을 보장할 수 있을 것으로 판단된다.
Conclusions
본 연구에서 NH3의 휘산은 온도와 강수량과 같은 기상인자 보다는 질소비료의 시용과 관련성이 더 높은 것으로 조사되었다. FeSO4는 토양의 pH를 저감시켜 NH4+가 NH3로 휘산되는 과정을 저해하여 배추 재배기간 동안 NH3의 누적배출량을 저감시키는 효과를 나타냈다. 또한 FeSO4의 시용량 증가에 따른 배추의 수량 감소는 발생하지 않았다. FeSO4를 110 kg ha-1로 시용 시 배추의 최대수량을 얻었을 수 있었으며 배추 재배기간 동안 NH3 누적배출량을 10.2% 감소시키는 효과를 얻었을 수 있었다. 따라서 FeSO4는 밭토양에 적정량으로 시용된다면 PM2.5의 원인물질인 NH3의 발생량을 저감하면서 작물의 생산성을 보장할 수 있는 좋은 토양개량제로 활용될 수 있을 것으로 판단된다.